Химия - удивительная наука. Столько невероятного можно обнаружить в, казалось бы, обычных вещах.
Всё материальное, что окружают нас повсюду, существует в нескольких агрегатных состояниях: газы, жидкости и твёрдые тела. Учёные выделили ещё и 4-е - плазму. При определённой температуре какое-либо вещество может переходить из одного состояние в другое. Например, вода: при нагревании свыше 100, из жидкой формы, превращается в пар. При температуре ниже 0 переходит в следующее агрегатную структуру - лёд.
Весь материальный мир имеет в своём составе массу одинаковых частиц, которые между собой связаны. Эти мельчайшие элементы строго выстраиваются в пространстве и образуют так называемый пространственный каркас.
Определение
 Кристаллическая решётка - особая структура твёрдого вещества, при которой частицы стоят в геометрически строгом порядке в пространстве. В ней можно обнаружить узлы - места, где расположены элементы: атомы, ионы и молекулы и межузловое пространство.
Кристаллическая решётка - особая структура твёрдого вещества, при которой частицы стоят в геометрически строгом порядке в пространстве. В ней можно обнаружить узлы - места, где расположены элементы: атомы, ионы и молекулы и межузловое пространство.
Твёрдые вещества , в зависимости от диапазона высоких и низких температур, являются кристаллическими или аморфными - они характеризуются отсутствием определённой температуры плавления. При воздействии повышенных температур они размягчаются и постепенно переходят в жидкую форму. К такого рода веществам относятся: смола, пластилин.
В связи с этим можно поделить на несколько видов:
- атомную;
- ионную;
- молекулярную;
- металлическую.
Но при различных температурах одно вещество может иметь различные формы и проявлять многообразные свойства. Это явление называется аллотропной модификацией.
Атомный тип
В этом типе в узлах расположены атомы того или иного вещества, которые связаны ковалентными связями. Этот вид связи образован парой электронов двух соседних атомов. Благодаря этому они связываются равномерно и в строгом порядке.
Вещества с атомной кристаллической решёткой характеризуются следующими свойствами: прочность и большая температура плавления. Такой тип связи представлен у алмаза, кремния и бора .
Ионный тип
Противоположно заряженные ионы находятся на узлах, которые создают электромагнитное поле, характеризующее физические свойства вещества. К таковым будут относиться: электропроводность, тугоплавкость, плотность и твёрдость. Поваренная соль и нитрат калия характеризуются наличием ионной кристаллической решётки.
Не пропустите: механизм образования , конкретные примеры.
Молекулярный тип
В узлах такого типа находятся ионы, связанные между собой ван-дер-ваальсовыми силами. Благодаря слабым межмолекулярным связям такие вещества, например, лёд, двуокись углерода и парафин, характеризуются пластичностью, электро- и теплопроводностью.
Металлический тип
 В своём строении напоминает молекулярную, но имеет всё же более прочные связи. Отличие данного типа в том, что на её узлах находятся положительно заряженные катионы . Электроны, которые находятся в межузловом
пространстве, участвуют в образовании электрического поля. Они ещё носят название электрического газа.
В своём строении напоминает молекулярную, но имеет всё же более прочные связи. Отличие данного типа в том, что на её узлах находятся положительно заряженные катионы . Электроны, которые находятся в межузловом
пространстве, участвуют в образовании электрического поля. Они ещё носят название электрического газа.
Простые металлы и сплавы, характеризуются металлическим типом решётки. Для них характерно наличие металлического блеска, пластичность, тепло- и электропроводность. Они могут плавиться при различных температурах.
Твердые вещества, как правило, имеют кристаллическое строение. Оно характеризуется правильным расположением частиц в строго определенных точках пространства. При мысленном соединении этих точек пересекающимися прямыми линиями образуется пространственный каркас, который называюткристаллической решеткой . Точки, в которых размещены частицы, называются узлами кристаллической решетки . В узлах воображаемой решетки могут находиться ионы, атомы или молекулы. Они совершают колебательные движения. С повышением температуры амплитуда колебаний возрастает, что проявляется в тепловом расширении тел.
В зависимости от вида частиц и характера связи между ними различают 4 вида кристаллических решеток: ионные (NaCl, KCl), атомные, молекулярные и металлические.
Кристаллические решетки, состоящие из ионов, называются ионными . Их образуют вещества с ионной связью. Примером может служить кристалл хлорида натрия, в котором каждый ион натрия окружен 6 хлорид-ионами, а каждый хлорид-ион 6 ионами-натрия.
Кристаллическая решетка NaCl
Число ближайших соседних частиц, вплотную примыкающих к данной частице в кристалле или отдельной молекуле называется координационным число .
В решетке NaCl координационные числа обоих ионов равны 6. И так, в кристалле NaCl нельзя выделить отдельные молекулы соли. Их нет. Весь кристалл следует рассматривать как гигантскую макромолекулу, состоящую из равного числа ионов Na + и Cl - , Na n Cl n – где n большое число. Связи между ионами в таком кристалле весьма прочны. Поэтому вещества с ионной решеткой обладают сравнительно высокой твердостью. Они тугоплавки и малолетучи.
Плавление ионных кристаллов приводит к нарушению геометрически правильной ориентации ионов относительно друг друга и уменьшению прочности связи между ними. Поэтому расплавы их проводят электрический ток. Ионные соединения, как правило, легко растворяются в жидкостях, состоящих из полярных молекул, например, воде.
Кристаллические решетки, в узлах которых находятся отдельные атомы, называются атомными . Атомы в таких решетках соединены между собой прочными ковалентными связями. Примером может служить алмаз - одна из модификаций углерода. Алмаз состоит из атомов углерода, каждый из которых связан с 4 соседними атомами. Координационное число углерода в алмазе равно 4. Вещества с атомной кристаллической решеткой имеют высокую температуру плавления (у алмаза свыше 3500 о С), прочны и тверды, практически не растворимы в воде.
Кристаллические решетки, состоящие из молекул (полярных и неполярных), называются молекулярными . Молекулы в таких решетках соединены между собой сравнительно слабыми межмолекулярными силами. Поэтому вещества с молекулярной решеткой имеют малую твердость и низкую температуру плавления, нерастворимы или малорастворимы в воде, их растворы почти не проводят электрический ток. Примерами их являются лед, твердый СО 2 («сухой лед»), галогены, кристаллы водорода, кислорода, азота, благородных газов и др.
Валентность
Важной количественной характеристикой, показывающей число взаимодействующих между собой атомов в образовавшейся молекуле, является валентность – свойство атомов одного элемента присоединять определенное число атомов других элементов.
Количественно валентность определяется числом атомов водорода, которое данный элемент может присоединять или замещать. Так, например, в плавиковой кислоте (HF) фтор одновалентен, в аммиаке (NH 3) азот трехвалентен, в кремневодороде (SiH 4 – силан) кремний четырехвалентен и т.д.
Позже, с развитием представлений о строении атомов, валентность элементов стали связывать с числом неспаренных электронов (валентных), благодаря которым осуществляется связь между атомами. Таким образом, валентностьопределяется числом неспаренных электронов в атоме, принимающих участие в образовании химической связи (в основном или возбужденном состоянии). В общем случае валентность равна числу электронных пар, связывающих данный атом с атомами других элементов.
Вещество, как вам известно, может существовать в трёх агрегатных состояниях: газообразном, жидком и твёрдом (рис. 70). Например, кислород, который при обычных условиях представляет собой газ, при температуре -194 °С превращается в жидкость голубого цвета, а при температуре -218,8 °С затвердевает в снегообразную массу, состоящую из кристаллов синего цвета.
Рис. 70.
Агрегатные состояния воды
Твёрдые вещества делят на кристаллические и аморфные.
Аморфные вещества не имеют чёткой температуры плавления - при нагревании они постепенно размягчаются и переходят в текучее состояние. К аморфным веществам относится большинство пластмасс (например, полиэтилен), воск, шоколад, пластилин, различные смолы и жевательные резинки (рис. 71).

Рис. 71.
Аморфные вещества и материалы
Кристаллические вещества характеризуются правильным расположением составляющих их частиц в строго определённых точках пространства. При соединении этих точек прямыми линиями образуется пространственный каркас, называемый кристаллической решёткой. Точки, в которых размещены частицы кристалла, называют узлами решётки.
В узлах воображаемой кристаллической решётки могут находиться одноатомные ионы, атомы, молекулы. Эти частицы совершают колебательные движения. С повышением температуры размах этих колебаний возрастает, что приводит, как правило, к тепловому расширению тел.
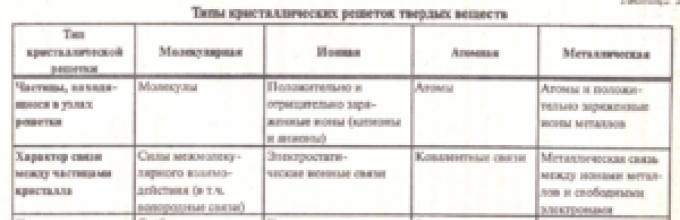
В зависимости от типа частиц, расположенных в узлах кристаллической решётки, и характера связи между ними различают четыре типа кристаллических решёток: ионные, атомные, молекулярные и металлические (табл. 6).
Таблица 6
Положение элементов в Периодической системе Д. И. Менделеева и типы кристаллических решёток их простых веществ

Простые вещества, образованные элементами, не представленными в таблице, имеют металлическую решётку.
Ионными называют кристаллические решётки, в узлах которых находятся ионы. Их образуют вещества с ионной связью, которой могут быть связаны как простые ионы Na + , Cl - , так и сложные , ОН - . Следовательно, ионные кристаллические решётки имеют соли, основания (щёлочи), некоторые оксиды. Например, кристалл хлорида натрия построен из чередующихся положительных ионов Na + и отрицательных Сl - , образующих решётку в форме куба (рис. 72). Связи между ионами в таком кристалле очень прочны. Поэтому вещества с ионной решёткой обладают сравнительно высокой твёрдостью и прочностью, они тугоплавки и нелетучи.

Рис. 72.
Ионная кристаллическая решётка (хлорид натрия)
Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы. В таких решётках атомы соединены между собой очень прочными ковалентными связями.

Рис. 73.
Атомная кристаллическая решётка (алмаз)
Такой тип кристаллической решётки имеет алмаз (рис. 73) - одно из аллотропных видоизменений углерода. Огранённые и отшлифованные алмазы называют бриллиантами. Их широко применяют в ювелирном деле (рис. 74).

Рис. 74.
Две императорские короны с алмазами:
а - корона Британской империи; б - Большая императорская корона Российской империи
К веществам с атомной кристаллической решёткой относятся кристаллические бор, кремний и германий, а также сложные вещества, например такие, как кремнезем, кварц, песок, горный хрусталь, в состав которых входит оксид кремния (IV) SiO 2 (рис. 75).

Рис. 75.
Атомная кристаллическая решётка (оксид кремния (IV))
Большинство веществ с атомной кристаллической решёткой имеют очень высокие температуры плавления (например, у алмаза она свыше 3500 °С, у кремния - 1415 °С, у кремнезёма - 1728 °С), они прочны и тверды, практически нерастворимы.
Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Химические связи в этих молекулах могут быть и ковалентными полярными (хлороводород НСl, вода Н 2 0), и ковалентными неполярными (азот N 2 , озон 0 3). Несмотря на то что атомы внутри молекул связаны очень прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного притяжения. Поэтому вещества с молекулярными кристаллическими решётками имеют малую твёрдость, низкие температуры плавления, летучи.
Примерами веществ с молекулярными кристаллическими решётками являются твёрдая вода - лёд, твёрдый оксид углерода (IV) С) 2 - «сухой лёд» (рис. 76), твёрдые хлороводород НСl и сероводород H 2 S, твёрдые простые вещества, образованные одно- (благородные газы: гелий, неон, аргон, криптон), двух- (водород Н 2 , кислород O 2 , хлор Сl 2 , азот N 2 , иод 1 2), трёх- (озон O 3), четырёх- (белый фосфор Р 4), восьмиатомными (сера S 7) молекулами. Большинство твёрдых органических соединений имеют молекулярные кристаллические решётки (нафталин, глюкоза, сахар).

Рис. 76.
Молекулярная кристаллическая решётка (углекислый газ)
Вещества с металлической связью имеют металлические кристаллические решётки (рис. 77). В узлах таких решёток находятся атомы и ионы (то атомы, то ионы, в которые легко превращаются атомы металла, отдавая свои внешние электроны в общее пользование). Такое внутреннее строение металлов определяет их характерные физические свойства: ковкость, пластичность, электро- и теплопроводность, металлический блеск.

Рис. 77.
Металлическая кристаллическая решётка (железо)
Лабораторный опыт № 13
Ознакомление с коллекцией веществ с разным типом кристаллической решётки. Изготовление моделей кристаллических решёток
-
Ознакомьтесь с коллекцией выданных вам образцов веществ. Запишите их формулы, охарактеризуйте физические свойства и на их основе определите тип кристаллической решётки.
Соберите модель одной из кристаллических решёток.
Для веществ, имеющих молекулярное строение, справедлив открытый французским химиком Ж. Л. Прустом (1799-1803) закон постоянства состава. В настоящее время этот закон формулируют так:
Закон Пруста - один из основных законов химии. Однако для веществ немолекулярного строения, например ионного, этот закон не всегда справедлив.
Ключевые слова и словосочетания
- Твёрдое, жидкое и газообразное состояния вещества.
- Твёрдые вещества: аморфные и кристаллические.
- Кристаллические решётки: ионные, атомные, молекулярные и металлические.
- Физические свойства веществ с различными типами кристаллических решёток.
- Закон постоянства состава.
Работа с компьютером
- Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
- Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока - сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
Вопросы и задания
- В каком агрегатном состоянии будет находиться кислород при -205 °С?
- Вспомните произведение А. Беляева «Продавец воздуха» и охарактеризуйте свойства твёрдого кислорода, используя его описание, приведённое в книге.
- К какому типу веществ (кристаллические или аморфные) относятся пластмассы? Какие свойства пластмасс лежат в основе их промышленного применения?
- К какому типу относится кристаллическая решетка алмаза? Перечислите характерные для алмаза физические свойства.
- К какому типу относится кристаллическая решетка иода? Перечислите характерные для иода физические свойства.
- Почему температура плавления металлов изменяется в очень широких пределах? Для подготовки ответа на этот вопрос используйте дополнительную литературу.
- Почему изделие из кремния при ударе раскалывается на кусочки, а изделие из свинца только расплющивается? В каком из указанных случаев происходит разрушение химической связи, а в каком - нет? Почему?
Cтраница 1
Молекулярные кристаллические решетки и соответствующие им молекулярные связи образуются преимущественно в кристал-дах тех веществ, в молекулах которых связи являются ковалент-ными. При нагревании связи между молекулами легко разрушаются, поэтому вещества с молекулярными решетками обладают низкими температурами плавления.
Молекулярные кристаллические решетки образуются из полярных молекул, между которыми возникают силы взаимодействия, так называемые ван-дер-ваальсовы силы, имеющие электрическую природу. В молекулярной решетке они осуществляют довольно слабую связь. Молекулярную кристаллическую решетку имеют лед, природная сера и многие органические соединения.
Молекулярная кристаллическая решетка иода показана на рис. 3.17. Большинство кристаллических органических соединений имеют молекулярную решетку.
Узлы молекулярной кристаллической решетки образованы молекулами. Молекулярную решетку имеют, например, кристаллы водорода, кислорода, азота, благородных газов, диоксида углерода, органических веществ.
Наличие молекулярной кристаллической решетки твердой фазы является здесь причиной незначительной адсорбции ионов из маточного раствора, а следовательно, и гораздо более высокой чистоты осадков по сравнению с осадками, для которых характерна ионная кристал. Поскольку осаждение в этом случае происходит в оптимальной области кислотности, различной для ионов, осаждаемых этим реактивом, оно находится в зависимости от значения соответствующих констант устойчивости комплексов. Этот факт позволяет, регулируя кислотность раствора, достигать селективного, а иногда даже специфического осаждения определенных ионов. Подобные результаты часто могут быть получены путем подходящего изменения доноркых групп в органических реактивах с учетом особенностей катионов-ком-плексообразователей, которые осаждаются.
В молекулярных кристаллических решетках наблюдается локальная анизотропия связей, а именно: внутримолекулярные силы очень велики по сравнению с межмолекулярными.
В молекулярных кристаллических решетках в узлах решетки находятся молекулы. Большинство веществ с ковалентной связью образуют кристаллы такого типа. Молекулярные решетки образуют твердые водород, хлор, двуокись углерода и другие вещества, которые при обычной температуре газообразны. Кристаллы большинства органических веществ также относятся к этому типу. Таким образом, веществ с молекулярно кристаллической решеткой известно очень много.
В молекулярных кристаллических решетках составляющие их молекулы связаны между собой при помощи относительно слабых ван-дер-ваальсовых сил, тогда как атомы внутри молекулы связаны значительно более сильной ковалентной связью. Поэтому в таких решетках молекулы сохраняют свою индивидуальность и занимают один узел кристаллической решетки. Замещение здесь возможно в том случае, если молекулы сходны между собой по форме и по размерам. Поскольку силы, связывающие молекулы, относительно слабы, то и границы замещения здесь значительно шире. Как показал Никитин , атомы благородных газов могут изоморфно замещать молекулы СО2, SO2, CH3COCH3 и другие в решетках этих веществ. Сходство химической формулы здесь оказывается не обязательным.
В молекулярных кристаллических решетках в узлах решетки находятся молекулы. Большинство веществ с ковалентной связью образуют кристаллы такого типа. Молекулярные решетки образуют твердые водород, хлор, двуокись углерода и другие вещества, которые при обычной температуре газообразны. Кристаллы большинства органических веществ также относятся к этому типу. Таким образом, веществ с молекулярной кристаллической решеткой известно очень много. Молекулы, находящиеся в узлах решетки, связаны друг с другом межмолекулярными силами (природа этих сил была рассмотрена выше; см. стр. Так как межмолекулярные силы значительно слабее сил химической связи, то молекулярные кристаллы легкоплавки, характеризуются значительной летучестью, твердость их невелика. Особенно низки температуры плавления и кипения у тех веществ, молекулы которых неполярны. Так, например, кристаллы парафина очень мягки, хотя ковалентные связи С-С в углеводородных молекулах, из которых состоят эти кристаллы, столь же прочны, как связи в алмазе. Кристаллы, образуемые благородными газами, также следует отнести к молекулярным, состоящим из одноатомных молекул, поскольку валентные силы в образовании этих кристаллов роли не играют, и связи между частицами здесь имеют тот же характер, что и в других молекулярных кристаллах; это обусловливает сравнительно большую величину межатомных расстояний в этих кристаллах.
| Схема регистрации дебаеграммм. |
В узлах молекулярных кристаллических решеток находятся молекулы, которые связаны друг с другом слабыми межмолекулярными силами. Такие кристаллы образуют вещества с ковалент-ной связью в молекулах. Веществ с молекулярной кристаллической решеткой известно очень много. Молекулярные решетки имеют твердые водород, хлор, диоксид углерода и другие вещества, которые при обычной температуре газообразны. Кристаллы большинства органических веществ также относятся к этому типу.
Существующее в природе, образовано большим числом одинаковых частиц, которые связаны между собою. Все вещества существуют в трёх агрегатных состояниях: газообразном, жидком и твёрдом. Когда затруднено тепловое движение (при низких температурах), а также в твердых веществах частицы строго ориентированы в пространстве, что проявляется в их точной структурной организации.
Кристаллическая решётка вещества - это структура с геометрически упорядоченным расположением частиц (атомы, молекулы либо ионы) в определённых точках пространства. В различных решетках различают межузловое пространство и непосредственно узлы - точки, в которых расположены сами частицы.
Кристаллическая решётка бывает четырех типов: металлическая, молекулярная, атомная, ионная. Типы решеток определяются в соответствии с видом частиц, расположенных в их узлах, а также характером связей между ними.
Кристаллическая решётка называется молекулярной в том случае, если в ее узлах располагаются молекулы. Они связаны между собой межмолекулярными сравнительно слабыми силами, называемые ван-дер-ваальсовыми, однако сами атомы внутри молекулы соединяются существенно более сильной либо неполярной). Молекулярная кристаллическая решетка свойственна хлору, твердому водороду, и другим веществам, являющимся газообразными при обычной температуре.
Кристаллы, которые образуют благородные газы, также имеют молекулярные решетки, состоящие из одноатомных молекул. Большинство твердых органических веществ имеют именно такую структуру. Число же которым свойственна молекулярная структура, весьма невелико. Это, например, твердые галогеноводороды, природная сера, лед, твердые простые вещества и некоторые другие.
При нагревании относительно слабые межмолекулярные связи разрушаются довольно легко, поэтому вещества с такими решетками имеют очень низкие температуры плавления и малую твердость, они нерастворимы либо малорастворимы в воде, растворы их практически не проводят электрический ток, характеризуются значительной летучестью. Минимальные температуры кипения и плавления - у веществ из неполярных молекул.
Металлической называется такая кристаллическая решетка, узлы которой сформированы атомами и положительными ионами (катионами) металла со свободными валентными электронами (отцепившимися от атомов при образовании ионов), беспорядочно движущимися в объеме кристалла. Однако эти электроны по существу являются полусвободными, так как могут беспрепятственно перемещаться только в рамках, которые ограничивает данная кристаллическая решетка.
Электростатические электроны и положительные ионы металлов взаимно притягиваются, чем объясняется стабильность металлической кристаллической решетки. Совокупность свободных движущихся электронов называют электронным газом - он обеспечивает хорошую электро- и При появлении электрического напряжения электроны устремляются к положительной частице, участвуя в создании электрического тока и взаимодействуя с ионами.
Металлическая кристаллическая решетка характерна, главным образом, для элементарных металлов, а также для соединений различных металлов друг с другом. Основные свойства, которые присущи металлическим кристаллам(механическая прочность, летучесть, достаточно сильно колеблются. Однако такие физические свойства, как пластичность, ковкость, высокая электро- и теплопроводность, характерный металлический блеск свойственны лишь исключительно кристаллам с металлической решеткой.