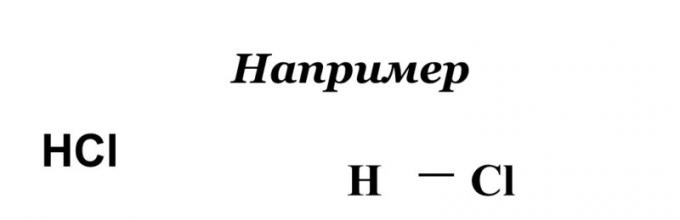| Одинарная (σ) | Двойная (σ+π) | Тройная (σ + π + π) |
| С–С С–Н С–О H–Cl | С=O С=С О=О | С≡С С≡N N≡N |
Гибридизация
Если атом связан с другими атомами ОДИНАКОВЫМИ СВЯЗЯМИ, но при их образовании участвуют орбитали разного типа, то используется метод ГИБРИДИЗАЦИИ.
Пример: Молекула СН 4 имеет форму правильного тетраэдра, в ней все 4 связи имеют одинаковую длину, прочность, находятся под одинаковыми углами друг к другу.
Однако у четырёхвалентного атома углерода электроны расположены на трёх р-орбиталях и одной s-орбитали. Они разные по энергии, форме и расположены в пространстве иначе.
Для объяснения используется понятие ГИБРИДИЗАЦИИ:
Из четырёх атомных орбиталей образуются 4 новых,
гибридных орбитали, которые в пространстве располагаются НА МАКСИМАЛЬНОМ УДАЛЕНИИ ДРУГ ОТ ДРУГА. Это правильный тетраэдр, углы между связями равны 109° 29´.
Так как в образовании четырёх связей участвуют одна s и три р-оболочки, то такой тип гибридизации обозначается sp 3
В зависимости от числа и типа орбиталей, которые принимают участие в гибридизации, отличают следующие типы гибридизации:
1) sp-гибридизация. Участвуют одна s-орбиталь и одна р-орбиталь. Молекула имеет линейную структуру, валентный угол – 180 0 .
2) sp 2 -гибридизация. Участвуют одна s-орбиталь и две р-орбитали. Молекула располагается в плоскости (концы гибридных орбиталей направлены к вершинам равностороннего треугольника), валентный угол – 120 0 .
3) sp 3 -гибридизация. Участвуют одна s-орбиталь и три р-орбитали. Молекула имеет тетраэдрическую форму, валентный угол – 109,28 0 .
Как определить тип гибридизации?
1. В гибридизации участвуют сигма-связи и НЕПОДЕЛЁННЫЕ ИОННЫЕ ПАРЫ.
2. Общее число участвующих орбиталей сигма-связей + электронных пар = числу гибридных орбиталей и определяет тип гибридизации.
Задание: определить тип гибридизации атома углерода в молекуле фосгена.
O=C – Cl
1) углерод образует 2 одинарные связи (это сигма-связи) и одну двойную связь (сигма+пи).Все 4 электрона углерода участвуют в образовании этих связей.
2) таким образом, в гибридизации примут участие ТРИ СИГМА-связи. Это sp 2 - гибридизация , молекула имеет форму плоского треугольника. Пи-связь располагается перпендикулярно плоскости этого треугольника.




Примеры. Определите тип химической связи между атомами в молекулах веществ: гидроксида натрия, серной кислоты, гидроксида мышьяка, сульфата натрия. Покажите стрелкой к какому элементу смещена электронная пара Какая связь более полярна? Каковы степени окисления атомов элементов?
Алгоритм выполнения 1.Изобразить графическую формулу. 2. Под каждым элементом проставить значение электроотрицательности из таблицы. 3. Стрелкой показать смещение электронной плотности. 4. Рассчитать разность относительных электроотрицательностей и указать тип связи (ионная, КП, КНП) 5. По направлению и количеству смещений электронной плотности определить степени окисления атомов элементов.

Пример выполнения NaOH Na OH 0,93 3,5 2, ОЭО(O-Na) ОЭО(O-Na)= 3,5 – 0,93=2,63 ОЭО(О-Н)= 3,5-2,1=1,4 ионная КП

Продолжение H 2 SO 4 S O O O O H H ОЭО(О-Н)=3,5-2.1=1.4 КП ОЭО(O-S)=3,5-2,6=0,9 КП



Определить тип гибридизации центрального атома в молекулах 1. СН 4 метана 2. NH 3 аммиака 3. Н 2 О Пример С НН Н Н Центральный атом – углерод. В(С)=4 3. …2s 2 2p s 1 2p 3

5. В формировании структуры молекулы участвуют одна s и три p- электронные орбитали. Все связи в молекуле метана одинарные -связи. Тип гибридизации sp 3. Все электронные облака участвующие в гибридизации одинаковы. Следовательно углы между ними одинаковы и =0. Молекула неполярна. Геометрическая форма тетраэдр. Ответ sp 3 -гибридизация =0, неполярная молекула
Молекула аммиака Рассуждая аналогично для молекулы аммиака: 1 N H H H 2. B(N)=3, …2s 2 2p 3: связи+электронная пара. 5. SР 3 - гибридизация. Электронные облака разного характера. Углы между ними неодинаковы. 0. Молекула полярна.

Молекула воды 2. Кислород В=2. :O: H H s 2 2p 4 4. В молекуле 2 -связи и две электроные пары. В формировании структуры молекулы участвуют s- и три p-электронные орбитали. Тип гибридизации sp 3. 0 (т.к. Углы между электронными облаками различны). Молекула полярна.
Взаимодействия между молекулами. Водородная связь Водородная связь – это особый вид взаимодействия между молекулами веществ. Водородная связь возникает между атомом водорода и другим более электроотрицательным атомом за счет сил электростатического притяжения по донорно-акцепторному механизму.
Вандерваальсово взаимодействие (межмолекулярное взаимодействие) 1873 год голландский ученый И. Ван-дер-Ваальс, предположил, что существуют силы, обусловливвающие притяжение между молекулами. Типы взаимодействия: 1) диполь-дипольное (ориентационное) Взаимодействие полярных молекул. 2) Индукционное. Взаимодействие полярных и неполярных молекул. Энергия этого вида взаимодействия слабее, чем ориентационного. 3)Дисперсионное. В неполярных молекулах (инертные газы) возникают флуктуации электронной плотности, в результате возникают мгновенные диполи, которые могут индуцировать соседние молекулы.


Общая и БИОорганическая химия
(конспект лекций)
Часть 2. Органическая химия
Для студентов 1 курса медицинского факультета специальности «Стоматология»
Издательство Российского университета дружбы народов,
У т в е р ж д е н о
РИС Ученого совета
Российского университета дружбы народов
Ковальчукова О.В., Авраменко О.В.
Общая и биоорганическая химия (конспект лекций). Часть 2. Органическая химия. Для студентов 1 курса медицинского факультета специальности «Стоматология». М.: Изд-во РУДН, 2010. 108 с.
Конспект лекций, читаемых для студентов 1 курса медицинского факультета специальности «Стоматология». Составлено в соответствии с программой курса "Общая и биоорганическая химия".
Подготовлено на кафедре общей химии.
© Ковальчукова О.В., Авраменко О.В.
© Издательство Российского университета дружбы народов, 2010
ВВЕДЕНИЕ
Биоорганическая химия – раздел химии, который тесно связан с такими специальными дисциплинами медицинских факультетов вузов, как биохимия, фармакология, физиология, молекулярная биология. Она является областью науки, изучающей строение и механизмы функционирования биологически активных молекул с позиций и представлений органической химии, определяющей закономерности во взаимосвязи строения и реакционной способности органических соединений.
Основное внимание в настоящем курсе лекций уделено классифицированию органических соединений по строению углеродного скелета и природе функциональных групп, закономерностям, связывающим химические строение органических молекул с характером их реакционных центров, связи их электронного и пространственного строения с механизмами химических превращений.
ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Органические соединения – это соединения углерода (кроме наиболее простых), в которых он проявляет валентность IV.
Органическая химия – это химия углеводородов и их производных.
Атом углерода в органических соединениях находится в возбужденном состоянии и имеет четыре неспаренных электрона:
6 С 1s 2 2s 2 2p 2 → 6 С* 1s 2 2s 1 2p 3
Атом углерода в возбужденном состоянии способен:
1) образовывать прочные связи с другими атомами углерода, что приводит к формированию цепей и циклов;
2) вследствие различного типа гибридизации орбиталей формировать простые, двойные и тройные связи между атомами углерода и с другими атомами (H, O, N, S, P и др.);
3) соединяться с четырьмя различными атомами, что приводит к образованию разветвленных углеродных цепочек.
Типы гибридизации атома углерода в органических соединениях
sp 3 – гибридизация
Все четыре валентные орбитали участвуют в гибридизации. Валентный угол 109 о 28’ (тетраэдр). Атомы углерода образуют только простые (σ) связи – соединение насыщенное.
sp 2 – гибридизация
Образуются три гибридные и одна негибридная орбиталь. Валентный угол 120 о (плоские структуры, правильный треугольник). Гибридные орбитали образуют σ–связи. Негибридные орбитали образуют p-связи. sp 2 –Гибридизация характерна для непредельных соединений с одной p - связью.
sp – гибридизация
Образуются две гибридные и две негибридные орбитали. Валентный угол 180 о (линейные структуры). Атом углерода в состоянии sp -гибридизации принимает участие в образовании двух двойных связей или одной тройной связи.
Теория строения органических соединений сформулирована в 1861 г А.М. Бутлеровым и включает следующие положения:
1. Все атомы, входящие в состав молекулы, связаны между собой в строго определенной последовательности в соответствии с их валентностями. Порядок соединения атомов в молекулу обусловливает ее химическое строение .
2. Свойства органических соединений зависят не только от качественного и количественного состава веществ, но и от порядка их соединения (химического строения молекулы).
3. Атомы в молекуле оказывают взаимное влияние друг на друга, т.е. свойства групп атомов в молекуле могут изменяться в зависимости от природы других атомов, входящих в состав молекулы. Группа атомов, определяющая химические свойства органических молекул, носит название функциональная группа .
4. Каждое органическое соединение имеет лишь одну химическую формулу. Зная химическую формулу, можно предсказать свойства соединения, а изучая на практике его свойства, установить химическую формулу.
Органическая молекула
Типы углеродного скелета :
Ациклический:
· разветвленный;
· нормальный (линейный).
Циклический:
· карбоциклический (цикл только из атомов углерода);
· гетероциклический (кроме атомов углерода в цикл входят некоторые другие атомы – азота, кислорода, серы).
Типы атомов углерода в углеводородной цепи:
Н 3 С-СН 2 -СН-С- СН 3
Первичные атомы углерода (соединены в цепи только с одним атомом углерода, является концевым);
Вторичный атом углерода (соединен с двумя соседними атомами углерода, находится в середине цепи);
Третичный атом углерода (находится на разветвлении углеродной цепи, соединен с тремя атомами углерода);
Четвертичный атом углерода (не имеет других заместителей, кроме атомов углерода).
Функциональная группа – особая группа атомов, которая определяет химические свойства соединений.
Примеры функциональных групп:
-ОН –гидроксильная группа (спирты, фенолы);
С=О – карбонильная группа (кетоны, альдегиды);
С - карбоксильнаягруппа (карбоновые кислоты);
-NH 2 – аминогруппа (амины);
-SH – тиольная группа (тиоспирты)
органическое соединение
| состав | свойства | химическое строение |
Атомы, входящие в состав органического соединения, могут по-разному соединяться в молекулы. Например, соединению состава С 2 Н 6 О может отвечать два химических соединения, имеющих разные физические и химические свойства:
Состав органического соединения – число атомов различных элементов входящих в его молекулу. Изомеры – соединения, имеющие одинаковый состав, но разное химическое строение. Изомеры обладают различными химическими свойствами.
Типы изомерии
СТРУКТУРНАЯ ИЗОМЕРИЯ
Изомерия углеродной цепи:
Изомерия положения кратных связей:
Межклассовая изомерия:
СТЕРЕОИЗОМЕРИЯ
Геометрическая (пространственная, цис-транс -изомерия соединений с двойными связями):
 |  |
| цис -бутен-2 | транс -бутен-2 |
Геометрическая изомерия возможна в том случае, если каждый из атомов углерода, участвующий в образовании двойной связи, имеет разные заместители. Так, для бутена-1 СН 2 =СН–СН 2 –СН 3 геометрическая изомерия невозможна, так как один из атомов углерода при двойной связи имеет два одинаковых заместителя (атомы водорода).
Геометрическая (пространственная, цис-транс -изомерия циклических предельных соединений):
Геометрическая изомерия возможна в том случае, если хотя бы два атома углерода, образующих цикл, имеют разные заместители.
Оптическая :
Оптическая изомерия – вид стереоизомерии, обусловленный хиральностью молекул. В природе имеются соединения, которые соотносятся как две руки одного человека. Одним из свойств этих соединений является их несовместимость со своим зеркальным отражением. Это свойство называется хиральностью (от греч. « сheir» – рука).
Оптическая активность молекул обнаруживается при действии на них поляризованного света. Если через раствор оптически активного вещества пропустить поляризованный луч света, то произойдет вращение плоскости его поляризации. Оптические изомеры обозначают, используя префиксы d-
В 1930 г. Слейтером и Л. Полингом была развита теория образования ковалентной связи за счет перекрывания электронных орбиталей – метод валентных связей. В основе этого метода лежит метод гибридизации, который описывает образование молекул веществ за счет «смешивания» гибридных орбиталей («смешиваются» не электроны, а орбитали).
ОПРЕДЕЛЕНИЕ
Гибридизация – смешение орбиталей и выравнивание их по форме и энергии. Так, при смешении s- и p- орбиталей получаем тип гибридизации sp, s- и 2-х p-орбиталей – sp 2 , s- и 3-х p-орбиталей – sp 3 . Существуют и другие типы гибридизации, например, sp 3 d, sp 3 d 2 и более сложные.
Определение типа гибридизации молекул с ковалентной связью
Определить тип гибридизации можно только для молекул с ковалентной связью типа АВ n , где n больше или равно двум, А – центральный атом, В – лиганд. В гибридизацию вступают только валентные орбитали центрального атома.
Определим тип гибридизации на примере молекулы BeH 2 .
Первоначально записываем электронные конфигурации центрального атома и лиганда, рисуем электронно-графические формулы.
Атом бериллия (центральный атом) имеет вакантные 2p-орбитали, поэтому, чтобы принять по одному электрону от каждого атома водорода (лиганд) для образования молекулы BeH 2 ему необходимо перейти в возбужденное состояние:

Образование молекулы BeH 2 происходит за счет перекрывания валентных орбиталей атома Be

* красным цветом обозначены электроны водорода, черным – бериллия.
Тип гибридизации определяют по тому, какие орбитали перекрылись, т.о., молекула BeH 2 находитс в sp – гибридизации.
Помимо молекул состава AB n , методом валентных связей можно определить тип гибридизации молекул с кратными связями. Рассмотрим на примере молекулы этилена C 2 H 4 . В молекуле этилена кратная двойная связь, которая образована и –связями. Чтобы определить гибридизацию, записываем электронные конфигурации и рисуем электронно-графические формулы атомов, входящих в состав молекулы:
6 C 2s 2 2s 2 2p 2

У атома углерода имеется еще одна вакантная p-орбиталь, следовательно, чтобы принять 4 атома водорода ему необходимо перейти в возбужденное состояние:

Одна p-орбиталь необходима для образования -связи (выделена красным цветом), поскольку -связь образуется за счет перекрывания «чистых» (негибридных) p — орбиталей. Остальные валентные орбитали идут в гибридизацию. Таким образом этилен находится в гибридизации sp 2 .
Определение геометрической структуры молекул
Геометрическую структуру молекул, а также катионов и анионов состава АВ n можно с помощью метода Гиллеспи. В основе этого метода – валентные пары электронов. На геометрическую структуру оказывают влияние не только электроны, участвующие в образовании химической связи, но и неподеленные электронные пары. Каждую неподеленную пару электронов в методе Гиллеспи обозначают Е, центральный атом – А, лиганд – В.
Если неподеленных электронных пар нет, то состав молекул может быть АВ 2 (линейная структура молекулы), АВ 3 (структура плоского треугольника), АВ4 (тетраэдрическая структура), АВ 5 (структура тригональной бипирамиды) и АВ 6 (октаэдрическая структура). От базисных структур могут быть получены производные, если вместо лиганда появляется неподеленная электронная пара. Например: АВ 3 Е (пирамидальная структура), АВ 2 Е 2 (угловая структура молекулы).
Чтобы определить геометрическую структуру (строение) молекулы необходимо определить состав частицы, для чего вычисляют количество неподеленных лектронных пар (НЕП):
НЕП = (общее число валентных электронов – число электронов, пошедших на образование связи с лигандами) / 2
На связь с H, Cl, Br, I, F уходит по 1-му электрону от А, на связь с O – по 2 электрона, а на связь с N – по 3 электрона от центрального атома.
Рассмотрим на примере молекулы BCl 3 . Центральный атом – B.
5 B 1s 2 2s 2 2p 1
НЕП = (3-3)/2 = 0, следовательно неподеленных электронных пар нет и молекула имеет структуру АВ 3 – плоский треугольник.
Подробно геометрическое строение молекул разного состава представлено в табл. 1.
Таблица 1. Пространственное строение молекул
|
Формула молекулы |
Тип гибридизации |
Тип молекулы |
Геометрия молекулы |
||
|
линейная |
|||||
|
треугольная |
|||||
|
тетраэдр |
|||||
|
тригональная пирамида |
|||||
|
тригональная бипирамида |
|||||
|
дисфеноид |
|||||
|
Т-образная |
|||||
|
линейная |
|||||
|
квадратная пирамида |
|||||
Примеры решения задач
ПРИМЕР 1
| Задание | Определите с помощью метода валентных связей тип гибридизации молекулы метана (CH 4) и его геометрическую структуру по методу Гиллеспи |
| Решение | 6 С 2s 2 2s 2 2p 2 |
Гибридизация атомных орбиталей – процесс, позволяющий понять, как атомы видоизменяют свои орбитали при образовании соединений. Так, что же такое гибридизация, и какие ее типы существуют?
Общая характеристика гибридизации атомных орбиталей
Гибридизация атомных орбиталей – это процесс, при котором смешиваются различные орбитали центрального атома, в результате чего образуются одинаковые по своим характеристикам орбитали.
Гибридизация происходит в процессе образования ковалентной связи.
Гибридная орбиталь имеет фору знака бесконечности или несимметричной перевернутой восьмерки, вытянутой в сторону от атомного ядра. Такая форма обусловливает более сильное, чем в случае чистых атомных орбиталей, перекрывание гибридных орбиталей с орбиталями (чистых или гибридных) других атомов и приводит к образованию более прочных ковалентных связей.

Рис. 1. Гибридная орбиталь внешний вид.
Впервые идею о гибридизации атомных орбиталей выдвинул американский ученый Л. Полинг. Он считал, что у вступающего в химическую связь атома имеются разные атомные орбитали (s-, p-, d-, f-орбитали), то в результате происходит гибридизация этих орбиталей. Суть процесса заключается в том, что из разных орбиталей образуются эквивалентные друг другу атомные орбитали.
Типы гибридизации атомных орбиталей
Существует несколько видов гибридизации:
- . Этот вид гибридизации происходит, когда смешиваются одна s-орбиталь и одна p-орбиталь. В результате образуются две полноценных sp-орбиталей. Эти орбитали расположены к атомному ядру таким образом, что угол между ними составляет 180 градусов.

Рис. 2. sp-гибридизация.
- sp2-гибридизация . Этот вид гибридизации происходит, когда смешиваются одна s-орбиталь и две p-орбитали. В результате происходит образование трех гибридных орбиталей, которые расположены в одной плоскости под углом 120 градусов друг к другу.
- . Этот вид гибридизации происходит, когда смешиваются одна s-орбиталь и три p-орбитали. В результате происходит образование четырех полноценных sp3-орбиталей. Эти орбитали направлены к вершине тетраэдра и располагаются друг к другу под углом 109,28 градусов.
sp3-гибридизация характерна для многих элементов, например, атома углерода и других веществ IVА группы (CH 4 , SiH 4 , SiF 4 , GeH 4 и др.)

Рис. 3. sp3-гибридизация.
Возможны также и более сложные виды гибридизации с участием d-орбиталей атомов.
Что мы узнали?
Гибридизация – сложный химический процесс, когда разные орбитали атома образуют одинаковые (эквивалентные) гибридные орбитали. Первым теорию гибридизации озвучил американец Л. Полинг. Выделяют три основных вида гибридизации: sp-гибридизация, sp2-гибридизация, sp3-гибридизация. Существуют также более сложные виды гибридизации, в которых участвуют d-орбитали.