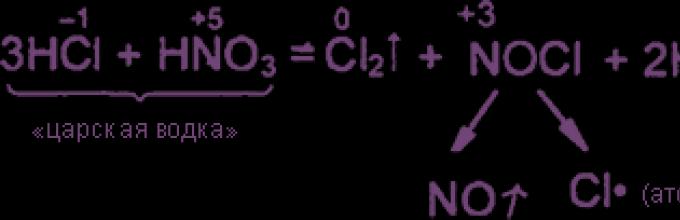Современные методы обеззараживания воды Хохрякова Елена Анатольевна
4.2.1. Хлор
Хлор является самым распространенным веществом, используемым для обеззараживания питьевой воды. Это объясняется его высокой эффективностью, простотой используемого технологического оборудования, дешевизной применяемого реагента – жидкого или газообразного хлора – и относительной простотой обслуживания.
Хлор легко растворяется в воде, после смешения газообразного хлора с водой в водном растворе устанавливается равновесие:
НСlО? Н + + ОСl -
Наличие хлорноватистой кислоты в водных растворах хлора и получающиеся в результате ее диссоциации анионы ОСl - обладают сильными бактерицидными свойствами. Хлорноватистая кислота почти в 300 раз более активна, чем гипохлорит-ионы ClO - . Объясняется это уникальной способностью HClO проникать в бактерии через их мембраны. Хлорноватистая кислота подвержена разложению на свету:
2HClO ? 2O + 2HCl ? О 2 + 2HCl
с образованием хлористоводородной кислоты и атомарного кислорода в качестве промежуточного вещества, который также является сильнейшим окислителем.
Обработку воды хлором осуществляют с помощью, так называемых, хлораторов, в которых газообразный (испаренный) хлор абсорбируют водой. Полученная хлорированная вода из хлоратора сразу подается к месту ее потребления. Несмотря на то что этот метод обработки воды и является наиболее распространенным, у него тоже есть ряд недостатков. Прежде всего, сложная транспортировка и хранение больших объемов жидкого высокотоксичного хлора. При такой организации процесса неизбежно присутствуют потенциально опасные стадии – прежде всего разгрузка емкостей с жидким хлором и его испарение для перевода в рабочую форму.
Создание рабочих запасов хлора на складах представляет опасность не только для рабочего персонала станции, но и для жителей расположенных рядом домов. Как альтернативный вариант хлорирования в последние годы все шире используют обработку воды раствором гипохлорита натрия (NaClO), этот метод находит применение как на промышленных станциях водоподготовки, так и на небольших объектах, в том числе в частных домах.
Cl 2 при об. Т - газ желто-зеленого цвета с резким удушающим запахом, тяжелее воздуха - в 2,5 раза, малорастворим в воде (~ 6,5 г/л); х. р. в неполярных органических растворителях. В свободном виде встречается только в вулканических газах.
Способы получения
Основаны на процессе окисления анионов Cl -
2Cl - - 2e - = Cl 2 0
Промышленный
Электролиз водных растворов хлоридов, чаще - NaCl:
2NaCl + 2Н 2 O = Cl 2 + 2NaOH + H 2
Лабораторные
Окисление конц. HCI различными окислителями:
4HCI + MnO 2 = Cl 2 + МпCl 2 + 2Н 2 O
16НСl + 2КМпО 4 = 5Cl 2 + 2MnCl 2 + 2KCl + 8Н 2 O
6HCl + КСlO 3 = ЗCl 2 + KCl + 3Н 2 O
14HCl + К 2 Сr 2 O 7 = 3Cl 2 + 2CrCl 3 + 2KCl + 7Н 2 O
Химические свойства
Хлор - очень сильный окислитель. Окисляет металлы, неметаллы и сложные вещества, превращаясь при этом в очень устойчивые анионы Cl - :
Cl 2 0 + 2e - = 2Cl -
Реакции с металлами
Активные металлы в атмосфере сухого газообразного хлора воспламеняются и сгорают; при этом образуются хлориды металлов.
Cl 2 + 2Na = 2NaCl
3Cl 2 + 2Fe = 2FeCl 3
Малоактивные металлы легче окисляются влажным хлором или его водными растворами:
Cl 2 + Сu = CuCl 2
3Cl 2 + 2Аu = 2AuCl 3
Реакции с неметаллами
Хлор непосредственно не взаимодействует только с O 2 , N 2 , С. С остальными неметаллами реакции протекают при различных условиях.
Образуются галогениды неметаллов. Наиболее важной является реакция взаимодействия с водородом.
Cl 2 + Н 2 =2НС1
Cl 2 + 2S (расплав) = S 2 Cl 2
ЗCl 2 + 2Р = 2РCl 3 (или РCl 5 - в избытке Cl 2)
2Cl 2 + Si = SiCl 4
3Cl 2 + I 2 = 2ICl 3
Вытеснение свободных неметаллов (Вr 2 , I 2 , N 2 , S) из их соединений
Cl 2 + 2KBr = Br 2 + 2KCl
Cl 2 + 2KI = I 2 + 2KCl
Cl 2 + 2HI = I 2 + 2HCl
Cl 2 + H 2 S = S + 2HCl
ЗСl 2 + 2NH 3 = N 2 + 6HCl
Диспропорционирование хлора в воде и водных растворах щелочей
В результате самоокисления-самовосстановления одни атомы хлора превращаются в анионы Cl - , а другие в положительной степени окисления входят в состав анионов ClO - или ClO 3 - .
Cl 2 + Н 2 O = HCl + НClO хлорноватистая к-та
Cl 2 + 2КОН =KCl + KClO + Н 2 O
3Cl 2 + 6КОН = 5KCl + KClO 3 + 3Н 2 O
3Cl 2 + 2Са(ОН) 2 = CaCl 2 + Са(ClO) 2 + 2Н 2 O
Эти реакции имеют важное значение, поскольку приводят к получению кислородных соединений хлора:
КClO 3 и Са(ClO) 2 - гипохлориты; КClO 3 - хлорат калия (бертолетова соль).
Взаимодействие хлора с органическими веществами
а) замещение атомов водорода в молекулах ОВ
б) присоединение молекул Cl 2 по месту разрыва кратных углерод-углеродных связей
H 2 C=CH 2 + Cl 2 → ClH 2 C-CH 2 Cl 1,2-дихлорэтан
HC≡CH + 2Cl 2 → Cl 2 HC-CHCl 2 1,1,2,2-тетрахлорэтан
Хлороводород и соляная кислота
Газообразный хлороводород
Физические и химические свойства
HCl - хлорид водорода. При об. Т - бесцв. газ с резким запахом, достаточно легко сжижается (т. пл. -114°С, т. кип. -85°С). Безводный НСl и в газообразном, и в жидком состояниях неэлектропроводен, химически инертен по отношению к металлам, оксидам и гидроксидам металлов, а также ко многим другим веществам. Это означает, что в отсутствие воды хлороводород не проявляет кислотных свойств. Только при очень высокой Т газообразный HCl реагирует с металлами, причем даже такими малоактивными, как Сu и Аg.
Восстановительные свойства хпорид-аниона в HCl также проявляются в незначительной степени: он окисляется фтором при об. Т, а также при высокой Т (600°С) в присутствии катализаторов обратимо реагирует с кислородом:
2HCl + F 2 = Сl 2 + 2HF
4HCl + O 2 = 2Сl 2 + 2Н 2 O
Газообразный HCl широко используется в органическом синтезе (реакции гидрохлорирования).
Способы получения
1. Синтез из простых веществ:
Н 2 + Cl 2 = 2HCl
2. Образуется как побочный продукт при хлорировании УВ:
R-H + Cl 2 = R-Cl + HCl
3. В лаборатории получают действием конц. H 2 SO 4 на хлориды:
H 2 SО 4 (конц.) + NaCl = 2HCl + NaHSО 4 (при слабом нагревании)
H 2 SО 4 (конц.) + 2NaCl = 2HCl + Na 2 SО 4 (при очень сильном нагревании)
Водный раствор HCl - сильная кислота (хлороводородная, или соляная)
HCl очень хорошо растворяется в воде: при об. Т в 1 л Н 2 O растворяется ~ 450 л газа (растворение сопровождается выделением значительного количества тепла). Насыщенный раствор имеет массовую долю HCl, равную 36-37 %. Такой раствор имеет очень резкий, удушающий запах.
Молекулы HCl в воде практически полностью распадаются на ионы, т. е. водный раствор HCl является сильной кислотой.
Химические свойства соляной кислоты
1. Растворенный в воде HCl проявляет все общие свойства кислот, обусловленные присутствием ионов Н +
HCl → H + + Cl -
Взаимодействие:
а) с металлами (до Н):
2HCl 2 + Zn = ZnCl 2 + H 2
б) с основными и амфотерными оксидами:
2HCl + CuO = CuCl 2 + Н 2 O
6HCl + Аl 2 O 3 = 2АlCl 3 + ЗН 2 O
в) с основаниями и амфотерными гидроксидами:
2HCl + Са(ОН) 2 = CaCl 2 + 2Н 2 О
3HCl + Аl(ОН) 3 = АlСl 3 + ЗН 2 O
г) с солями более слабых кислот:
2HCl + СаСО 3 = CaCl 2 + СO 2 + Н 3 O
HCl + C 6 H 5 ONa = С 6 Н 5 ОН + NaCl
д) с аммиаком:
HCl + NH 3 = NH 4 Cl
Реакции с сильными окислителями F 2 , MnO 2 , KMnO 4, KClO 3, K 2 Cr 2 O 7 . Анион Cl - окисляется до свободного галогена:
2Cl - - 2e - = Cl 2 0
Уравнения реакция см. "Получение хлора". Особое значение имеет ОВР между соляной и азотной кислотами:

Реакции с органическими соединениями
Взаимодействие:
а) с аминами (как органическими основаниями)
R-NH 2 + HCl → + Cl -
б) с аминокислотами (как амфотерными соедимнеиями)

Оксиды и оксокислоты хлора
Кислотные оксиды

Кислоты

Соли
Химические свойства
1. Все оксокислоты хлора и их соли являются сильными окислителями.
2. Почти все соединения при нагревании разлагаются за счет внутримолекулярного окисления-восстановления или диспропорционирования.

Хлорная известь
Хлорная (белильная) известь - смесь гипохлорита и хлорида кальция, обладает отбеливающим и дезинфицирующим действием. Иногда рассматривается как пример смешанной соли, имеющей в своем составе одновременно анионы двух кислот:

Жавелевая вода
Водный раствор хлорида и гапохлорита калия KCl + KClO + H 2 O
Как бы мы негативно ни относились к общественным уборным, природа диктует свои правила, и посещать их приходится. Помимо естественных (для данного места) запахов, еще одним привычным ароматом является хлорка, используемая для дезинфекции помещения. Свое название она получила из-за главного действующего вещества в ней - Cl. Дайте узнаем об этом химическом элементе и его свойствах, а также дадим характеристику хлора по положению в периодической системе.
Как был открыт этот элемент
Впервые хлорсодержащее соединение (HCl) было синтезировано в 1772 г. британским священником Джозефом Пристли.
Через 2 года его шведский коллега Карл Шееле сумел описать способ выделения Cl с помощью реакции между соляной кислотой и диоксидом марганца. Однако этот химик так и не понял, что в результате синтезируется новый химический элемент.
Почти 40 лет понадобилось ученым, чтобы научиться добывать хлор на практике. Впервые это было сделано британцем Гемфри Дэви в 1811 г. При этом он использовал другую реакцию, нежели его предшественники-теоретики. Дэви при помощи электролиза разложил на составляющие NaCl (известный большинству как кухонная соль).
Изучив полученное вещество, британский химик осознал, что оно является элементарным. После этого открытия Дэви не только назвал его - chlorine (хлорин), но и смог дать характеристику хлора, правда она была весьма примитивной.
Хлорин превратился в хлор (chlore) благодаря Жозефу Гей-Люссаку и в таком виде существует в французском, немецком, российском, белорусском, украинском, чешском, болгарском и некоторых других языках и сегодня. В английском по сей день употребляется название "хлорин", а в итальянском и испанском "хлоро".
Более подробно рассматриваемый элемент был описан Йенсом Берцелиусом в 1826 г. Именно он смог определить его атомную массу.
Что такое хлор (Cl)
Рассмотрев историю открытия данного химического элемента, стоит узнать о нем подробнее.
Название chlorine было образовано от греческого слова χλωρός («зеленый»). Дано оно было из-за желтовато-зеленоватого цвета данного вещества
Самостоятельно хлор существует как двухатомный газ Cl 2, однако в таком виде в природе он практически не встречается. Чаще он фигурирует в различных соединениях.
Помимо отличительного оттенка, для хлора характерен сладковато-едкий запах. Он является очень ядовитым веществом, поэтому при попадании в воздух и вдыхании человеком или животным способен в течение нескольких минут привести к их гибели (зависит от концентрации Cl).
Поскольку хлор тяжелее воздуха почти в 2,5 раза, он всегда будет находиться ниже его, то есть у самой земли. По этой причине при подозрении на наличие Cl следует забраться как можно выше, так как там будет меньшая концентрация данного газа.
Также, в отличие от некоторых других ядовитых веществ, хлорсодержащие обладают характерным цветом, что может позволить зрительно их идентифицировать и принять меры. Большинство стандартных противогазов помогают защитить органы дыхания и слизистые оболочки от поражения Cl. Однако для полной безопасности нужно принимать более серьезные меры, вплоть до нейтрализации ядовитого вещества.

Стоит отметить, что именно с применения немцами хлора как отравляющего газа в 1915 г. начало свою историю химическое оружие. В результате использования почти 200 тонн вещества было за несколько минут отравлено 15 тысяч человек. Треть из них умерла почти мгновенно, треть получила перманентные повреждения, и лишь 5 тысячам удалось спастись.
Почему же столь опасное вещество до сих пор не запрещено и ежегодно добывается миллионами тонн? Все дело в его особых свойствах, а чтобы понять их, стоит рассмотреть характеристику хлора. Проще всего это сделать с помощью таблицы Менделеева.
Характеристика хлора в периодической системе

Хлор как галоген
Помимо крайней токсичности и едкого запаха (характерных для всех представителей данной группы) Cl отлично растворяется в воде. Практическое подтверждение этому - добавление хлорсодержащих моющих средств в воду для бассейнов.
При контакте с влажным воздухом рассматриваемое вещество начинает дымиться.
Свойства Cl как неметалла
Рассматривая химическую характеристику хлора, стоит обратить внимание на его неметаллические свойства.
Он имеет способность образовывать соединения практически со всеми металлами и неметаллами. В качестве примера можно привести реакцию с атомами железа: 2Fe + 3Cl 2 → 2FeCl 3.
Часто для проведения реакций необходимо использовать катализаторы. В этой роли может выступать Н 2 О.
Нередко реакции с Cl носят эндотермический характер (поглощают тепло).
Стоит отметить, что в кристаллической форме (в виде порошка) хлор взаимодействует с металлами лишь при нагревании до высоких температур.
Реагируя с другими неметаллами (кроме О 2 , N, F, С и инертных газов), Cl образует соединения - хлориды.
При реакции с О 2 образуются крайне нестабильные и склонные к распаду оксиды. В них степень окисления Cl способна проявляться от +1 до +7.
При взаимодействии с F образуются фториды. Степень окисления их может быть разной.
Хлор: характеристика вещества с точки зрения его физических свойств
Помимо химических свойств, рассматриваемый элемент имеет и физические.

Влияние температуры на агрегатное состояние Cl
Рассмотрев физическую характеристику элемента хлора, мы понимаем, что он способен переходить в разные агрегатные состояния. Все зависит от температурного режима.
В нормальном состоянии Cl - это газ, обладающий высокими коррозийными свойствами. Однако он с легкостью способен сжижаться. На это влияет температура и давление. К примеру, если оно равно 8 атмосферам, а температура - +20 градусам по Цельсию, Cl 2 - кислотно-желтая жидкость. Данное агрегатное состояние он способен сохранять до +143 градусов, если давление также продолжает повышаться.

При достижении -32 °С состояние хлора перестает зависеть от давления, и он продолжает оставаться жидким.
Кристаллизация вещества (твердое состояние) происходит при -101 градусе.
Где в природе существует Cl
Рассмотрев общую характеристику хлора, стоит узнать, где же в природе может встречаться столь непростой элемент.
Из-за своей высокой реакционной активности он практически никогда не встречается в чистом виде (поэтому в начале изучения учеными этого элемента понадобились годы, чтобы научиться его синтезировать). Обычно Cl находится в составе соединений в различных минералах: галит, сильвин, каинит, бишофит и т. п.
Более всего он содержится в солях, добытых из морской или океанической воды.
Влияние на организм
При рассмотрении характеристики хлора уже было не раз сказано, что он крайне ядовит. При этом атомы вещества содержатся не только в минералах, но и практически во всех организмах, начиная от растений до человека.
Из-за особых свойств ионы Cl лучше других проникают сквозь мембраны клеток (поэтому более 80 % всего хлора в теле человека находится в межклеточном пространстве).
Вместе с К, Cl ответственен за регуляцию водно-солевого баланса и как следствие - за осмотическое равенство.
Несмотря на столь важную роль в организме, в чистом виде Cl 2 убивает все живое - от клеток до целых организмов. Однако в контролированных дозах и при кратковременном воздействии он не успевает причинить повреждений.

Ярким примером последнему утверждению служит любой бассейн. Как известно, воду в таких учреждениях дезинфицируют при помощи Cl. При этом, если человек редко посещает такое заведение (раз в неделю или в месяц) - маловероятно, что он пострадает от наличия данного вещества в воде. Однако работники таких учреждений, особенно те, кто почти весь день пребывают в воде (спасатели, инструкторы) часто страдают кожными заболеваниями или имеют ослабленный иммунитет.
В связи со всем этим после посещения бассейнов обязательно нужно принять душ - чтобы смыть возможные остатки хлора с кожи и волос.
Использования Cl человеком
Помня из характеристики хлора, что он является «капризным» элементом (когда дело доходит до взаимодействия с другими веществами), интересно будет узнать, что в промышленности он весьма часто используется.
В первую очередь с его помощью производится дезинфекция многих веществ.
Также Cl применяется при изготовлении некоторых видов пестицидов, что помогает спасать урожай от вредителей.
Способность этого вещества взаимодействовать почти со всеми элементами таблицы Менделеева (характеристика хлора как неметалла) помогает с его помощью добывать некоторые виды металлов (Ті, Та и Nb), а также известь и соляную кислоту.
Помимо всего вышеперечисленного Cl применяют при производстве промышленных веществ (поливинилхлорид) и медицинских препаратов (хлоргексидин).
Стоит упомянуть, что сегодня найдено более эффективное и безопасное дезинфицирующее средство - озон (О 3 ). Однако его производство более дорогостоящее, чем хлора, и этот газ еще более нестабилен, нежели хлор (краткая характеристика физических свойств в 6-7 п.). Поэтому применять озонирование вместо хлорирования пока могут позволить себе немногие.
Как добывается хлор
Сегодня известно немало способов для синтеза данного вещества. Все они делятся на две категории:
- Химические.
- Электрохимические.
В первом случае Cl получают вследствие химической реакции. Однако на практике они весьма затратные и малопроизводительны.
Поэтому в промышленности предпочитают электрохимические методы (электролиз). Их три: диафрагменный, мембранный и ртутный электролиз.
В данном разделе рассматриваются свойства, использование хлора, действие его на организм человека, поведение в атмосфере при выбросе, поражающие действия и классификация АХОВ, поведение хлора в зависимости от способа хранения, рассмотрены примеры аварий на станциях водоподготовки.
1.3.1 Хлор как ахов, его свойства и применение
Хлор к настоящему времени утратил значение как отравляющее вещество, однако весьма широко используется в различных отраслях производства. По токсическим свойствам хлор относится к аварийно-химическим опасным веществам (АХОВ). АХОВ - химические вещества или соединения, которые при проливе или выбросе из емкости в окружающую среду способны вызвать массовое поражение людей и животных, заражение воздуха, почвы, воды, растений и различных материальных ценностей выше допустимых значений. Таких АХОВ по мере расширения производства с каждым годом становится все больше. На сегодняшний день в системе РСЧС в перечень АХОВ включены более 34 веществ.
Согласно клинической классификации хлор является АХОВ первой группы – веществом, обладающим преимущественно удушающим поражающим действием с выраженным прижигающим действием.
Физико-химические
свойства.
Хлор – зеленовато желтый газ с резким
удушающим запахом. Плохо растворяется
в воде, хорошо – в некоторых органических
растворителях. В практических условиях
растворимость хлора в воде незначительна
и составляет 3 кг на 1 т воды. При обычном
давлении сжижается при температуре –
34°С, образуя маслянистую жидкость
желтовато зелёного цвета, затвердевающую
при минус 101°С. Твёрдый хлор это бледно
жёлтые кристаллы. Под давлением хлор
сжижается уже при обычных температурах.
Температура кипения сжиженного хлора
–34,1°С, следовательно, даже зимой хлор
находится в газообразном состоянии.
При испарении образует с водяными парами
белый туман. Один килограмм жидкого
хлора дает 0,315 м 3
газа. Хорошо адсорбируется активным
углём. Химически очень активен. 
Пожаро- и взрывоопасность хлора. Негорюч, но пожароопасен, поддерживает горение многих органических веществ. В смеси с водородом взрывоопасен. При нагревании ёмкости взрывается.
Действие
хлора на организм.
По физиологическому действию на организм
хлор относится к группе веществ удушающего
действия. В момент контакта он оказывает
сильное раздражающее действие на
слизистую оболочку дыхательных путей
и глаза. Признаки поражения наступают
сразу после воздействия, поэтому хлор
является быстродействующим АХОВ.
Проникая в глубокие дыхательные пути,
хлор разрушает лёгочную ткань, вызывая
отёк лёгких. В зависимости от концентрации
(токсодозы) хлора степень тяжести
отравления может быть различной. При
воздействии хлора уже в незначительных
концентрациях наблюдается покраснение
коньюктивы глаз, мягкого нёба и глотки,
а также бронхит, лёгкая одышка, охриплость,
чувство сдавливания в груди. Пребывание
в атмосфере, содержащей хлор в концентрациях
1,5–2 г/м 3 ,
сопровождается появлением болевых
ощущений в верхних дыхательных путях,
жжением и болью за грудиной (чувство
сильного сдавливания в груди), жжением
и резью в глазах, слезотечением,
мучительным сухим кашлем. Через 2–4 ч
появляются признаки отёка лёгких.
Увеличивается одышка, учащается пульс,
начинается отделение пенистой жёлтоватой
или красноватой мокроты.
Воздействие
высоких концентраций хлора в течение
10–15 мин может привести к развитию
химического ожога лёгких и смерти. При
вдыхании хлора в очень высоких
концентрациях смерть наступает в течение
нескольких минут из за паралича
дыхательного центра. Антидота
против хлора не существует.
Предельно допустимая концентрация
хлора в воздухе рабочей зоны
производственного помещения составляет
1 мг/м 3 ,
однако человек начинает ощущать хлор
в атмосферном воздухе при превышении
концентрации 3 мг/м 3 .
Следовательно, если чувствуется резкий
удушливый запах хлора, то работать без
средств защиты уже опасно. Раздражающее
действие возникает при концентрации
около 10 мг/м 3 .
Воздействие 100–200 мг/м 3
хлора в течение 30–60 минут опасно для
жизни. Предельно допустимая концентрация
хлора в атмосферном воздухе населённых
пунктов равна: среднесуточная 0,03 мг/м 3 ;
максимальная разовая 0,1 мг/м 3 .

Признаки поражения хлором. Сильное жжение, резь в глазах; слезотечение; учащённое дыхание; мучительный сухой кашель; сильное возбуждение; страх; в тяжёлых случаях остановка дыхания. При утечке или розливе хлора нельзя прикасаться к пролитому веществу, так как оставшийся в проливе хлор захолаживается до температуры -34°С.
Использование. Находит широкое применение для отбеливания тканей и бумажной массы, в производстве пластмасс, каучука, пестицидов, дихлорэтана, в цветной металлургии, а также в коммунально-бытовом хозяйстве для обеззараживания воды. Хлор хранят и перевозят к местам потребления только в сжиженном состоянии. Наиболее распространённым способом хранения и транспортировки жидкого хлора является хранение под давлением, соответствующим давлению насыщенных паров хлора при температуре окружающей среды. Обычно он хранится в цилиндрических (10–250 м 3) и шаровых (600–2000 м 3) резервуарах в сжиженном состоянии под давлением собственных паров, величина которого зависит от температуры жидкого хлора. При температуре 25°С оно составляет 8 кгс/см 2 , а при температуре 60°С – 18 кгс/см 2 . Сжиженный хлор перевозят в железнодорожных цистернах, контейнерах и баллонах, которые одновременно могут являться временными хранилищами.
Поведение
в атмосфере.
При разрушении емкости происходит
бурное (в зависимости от давления)
испарение хлора. Доля мгновенно
испарившегося хлора зависит от температуры
хранящегося жидкого хлора. Чем выше его
температура, тем большая доля хлора
практически мгновенно испаряется при
аварийном выбросе (20% при 20° С и 30% при
40°С). При этом образуется так называемое
первичное облако с концентрациями,
значительно превышающими смертельные
концентрации. Продолжительность
поражающего действия первичного облака
хлора на небольших удалениях от места
аварии будет составлять от нескольких
десятков секунд до нескольких минут.
Вторичное облако, образующееся при
испарении хлора с площади розлива,
характеризуется концентрацией этого
вещества в нем на 2–3 порядка ниже, чем
в первичном облаке. Однако продолжительность
действия в этом облаке хлора значительно
больше и определяется временем испарения
разливающейся жидкости. Испарение идет
за счет тепла поддона или подстилающей
поверхности, а также окружающего воздуха.
Время испарения зависит от количества
вещества, характера разлива: в поддон
или свободно (в обваловку) и от
метеорологических условий. Испарение
может длиться несколько часов и даже
суток.
Газообразный хлор в 2,5 раза
тяжелее воздуха, поэтому облако хлора
перемещается по направлению ветра
близко к земле. Обладает хорошей
проникающей способностью в негерметичные
сооружения. Может скапливаться в низких
участках местности, подвалах домов,
колодцах, тоннелях и защитных сооружениях,
не оборудованных в противохимическом
отношении. За внешнюю границу зоны
заражения принимается линия средней
пороговой токсодозы, вызывающей начальные
симптомы поражения (составляет 0,6 ).

В промышленных масштабах хлор получают вместе с гидроксидом натрияиводородомпутёмэлектролизараствораповаренной соли:
2NaCl + 2H 2 О → H 2 + Cl 2 + 2NaOH
Анод: 2Cl - - 2е - → Cl 2 0
Катод: 2H 2 O + 2e - → H 2 + 2OH -
На станциях водоподготовки хлор хранится в специальных «танках», или закачивается в стальные баллоны высокого давления. Баллоны с жидким хлором под давлением имеют специальную окраску - болотный цвет. Следует отметить, что при длительной эксплуатации баллонов с хлором, в них накапливается чрезвычайно взрывчатый треххлористый азот, и поэтому время от времени баллоны с хлором должны проходить плановую промывку и очистку от хлорида азота.
ПДК хлора в атмосферном воздухе следующие: среднесуточная - 0,03 мг/м³; максимально разовая - 0,1 мг/м³; в рабочих помещениях промышленного предприятия - 1 мг/м³.
Цель урока: Сформировать представление о хлоре как химическом элементе и простом веществе.
Задачи урока:
Образовательные:
1. Рассмотреть положение галогенов в Периодической системе химических элементов Д.И. Менделеева.
2. Ознакомить учащихся с нахождением хлора в природе и способами его получения.
3. Сформировать знания о физических и химических свойствах хлора.
4. Охарактеризовать области применения хлора и отметить его токсичность.
Воспитательные:
1. Воспитание чувства сопереживания, взаимопомощи через работу в группах.
2. Формирование экологической грамотности через учебный материал о применении хлора.
Развивающие:
1. Развитие коммуникативных, эмоциональных качеств личности через работу в группе.
2. Развивать способность делать выводы через выполнение заданий групп.
Тип урока: изучение нового материала.
Форма обучения: групповая, индивидуальная, фронтальная.
Методы урока: словесные, наглядные, самостоятельные.
План урока.
- Организационный момент – 1 мин.
- Актуализация знаний – 4 мин.
- Изучение нового материала – 25 мин.
- Закрепление изученного – 12 мин.
- Подведение итогов урока и домашнее задание – 3 мин.
Ход урока:
Организационный момент
- Приветствие.
Вводное слово учителя:
– Ребята, чем пахнет водопроводная вода?
– А чем пахнет на кухне, когда раковину чистят “белизной”?
– Чем мы солим суп?
– Что находится в желудке для переваривания пищи?
Таким образом, с каким элементом мы сегодня познакомимся на уроке? (Хлором).
Хлор является представителем галогенов (от греч halos – соль и genes – рождающий).
Актуализация знаний
- Определите местоположение галогенов в ПС Д.И. Менделеева, назовите их.
- Охарактеризуйте особенности строения атомов галогенов и электронную конфигурацию внешнего слоя.
- Какие свойства проявляют галогены в химических реакциях?
- Как изменяется окислительная способность галогенов с увеличением порядкового номера?
- Назвать самый активный галоген-неметалл? Почему?
Изучение нового материала
Постановка цели урока учащимися (с чем на уроке мы сегодня познакомимся?).
Новый материал изучается при работе в группах по инструктивным карточкам (12 минут). Приложение 1
Отчёт о работах в группах..
Заполнение таблицы в тетради (13 мин).
Закрепление изученного материала
CL 2 ->HCL->NaCL->AgCL
Тест “Хлор”
Тест выдан каждому ученику.
Вариант 1
1. Какая электронная конфигурация внешнего
энергетического уровня соответствует атому
хлора?
а) 2s
22p
6; б) 2s
22p
3; в) 3s
23p
5; г) 2s
22p
5.
2. Хлор впервые получил
а) А. Авогадро; б) А.Беккерель; в) К. Шееле; г) Г.
Кавендиш.
3. Галоген, обладающий наибольшим значением
электроотрицательности - это
а) I; б) Br; в) CL; г) F.
4. Положительную степень окисления хлор
проявляет в соединении
а) HCLO; б) KCLO 3 ; в) HCL; г) Cl 2 O 7 .
5.
Объём хлороводорода (н.у.)
полученного при сжигании 10л водорода в хлоре,
равен
а) 22,4 л; б) 10 л; в) 20 л; г) 44,8 л.
Вариант 2
1. Степень окисления –1 хлор проявляет в
соединении:
а) HCL; б) CL 2 ; в) Cl 2 O 7 ; г) KCLO 3 .
2. Хлор при обычных условиях:
а) бесцветный газ с резким удушливым запахом;
б) газ жёлто-зелёного цвета с резким удушливым
запахом;
в) жидкость красно-бурого цвета;
г) кристаллы темно-фиолетового цвета.
3. На наружном энергетическом уровне атомов
галогенов находится:
а) два s-электрона и пять р-электронов;
б) один s-электрон;
в) пять р-электронов;
г) два s-электрона и шесть р-электронов.
4. Объём хлора (н.у) затраченного на получение
2л хлороводорода, равен
а) 2 л; б) 22.4 л; в) 1 л; г) 44,8 л.
5. Галоген, обладающий наименьшим значением
электроотрицательности-это
а) I; б) Br; в) CL; г) F.
6. Установите соответствие между химической формулой соединения и степенью окисления хлора в нем.
Тесты сдают на проверку учителю.
Домашнее задание.
П. 46, 47, стр. 164 задача №2 (учебник Г.Е Рудзитис и Ф.Г.Фельдман химия 8).
Подведение итогов урока. Рефлексия.
На партах лежат сигнальные карточки трех цветов: красная – “всё понятно”, зеленая – “есть затруднения”, синяя – “нужна помощь”. Выберите карточки по мере вашего усвоения материала, подпишите их и сдайте.