Альдегиды- класс органических соединений, содержащих карбонильную группу -СОННазвание альдегидов происходит от названия углеводородных радикалов с добавлением суффикса -аль Общая формула предельных альдегидов СnH2n+1COH. Номенклатура и изомерия
Номенклатура этих двух групп соединений строится по-разному . Тривиальные названия альдегидов связывают их с тривиальными названиями кислот, в которые они переходят при окислении
Из кетонов лишь немногие имеют тривиальные названия (например, ацетон). Для них широко используется радикально-функциональная номенклатура , в которой названия кетонов даются с использованием названий радикалов, связанных с карбонильной группой. По номенклатуре ИЮПАК названия альдегидов производятся от названия углеводорода с тем же числом атомов углерода путём добавления окончания –аль .Длякетонов эта номенклатура требует окончания –он . Цифрой обозначается положение функциональной группы в цепи кетона.
| Соединение | Названия по триви-альной и радикально-функциональной номенклатурам | Названия по номенклатуре ИЮПАК |
| муравьиный альдегид; формальдегид | метаналь | |
| уксусный альдегид; ацетальдегид | этаналь | |
| пропионовый альдегид | пропиональ | |
| масляный альдегид | бутаналь | |
| изомасляный альдегид | метилпропаналь | |
| | валериановый альдегид | пентаналь |
 | изовалериановый альдегид | 3-метилбутаналь |
| ацетон; диметилкетон | пропанон | |
| метилэтилкетон | бутанон | |
| метилпропилкетон | пентанон-2 | |
| | метилизопропилкетон | 3-метилбутанон-2 |
Изомерия альдегидов и кетонов полностью отражается номенклатурой и комментарий не требует. Альдегиды и кетоны с одинаковым числом атомов углерода являются изомерами . Например:

Способы получения – Окисление или каталитическое дегидрирование первичных спиртов до альдегидов, вторичных – до кетонов . Реакции эти уже упоминались при рассмотрении химических свойств спиртов.
– Пиролиз кальциевых или бариевых солей карбоновых кислот, одна из которых – соль муравьиной кислоты, даёт альдегиды.
– Гидролиз геминальных (заместители у одного углерода) дигалогеналканов
– Гидратация ацетилена и его гомологов протекает в присутствии сульфата ртути (реакция Кучерова) или над гетерогенным катализатором
Физические свойства. Муравьиный альдегид – газ. Остальные низшие альдегиды и кетоны – жидкости, плохо растворимые в воде. Альдегиды имеют удушливый запах. Кетоны пахнут обычно приятно. 1. Р. Окисления.Альдегиды легко окисляются до карбоновых кислот. Окислителями могут служить гидроксид меди (II), оксид серебра, кислород воздуха:
![]()
Ароматические альдегиды окисляются труднее алифатических. Кетоны, как было сказано выше, окисляются труднее альдегидов. Окисление кетонов проводится в жестких условиях, в присутствии сильных окислителей. Образуются в результате смеси карбоновых кислот. При этом образуется металлическое серебро. Раствор оксида серебра готовят непосредственно перед опытом:

Альдегиды также восстанавливают свежеприготовленный аммиачный раствор гидроксида меди (II), обладающий светло-голубой окраской (реактив Фелинга), до желтого гидроксида меди (I), который при нагревании разлагается с выделением ярко-красного осадка оксида меди (I). СН3-СН=О + 2Cu(ОН)2 - СН3СООН+2CuОН+Н2О 2CuOH->Cu2O+H2O
2. Р. Присоединения. Гидрирование - присоединение водорода.Карбонильные соединения восстанавливаются до спиртов водородом, алюмогидридом лития, боргидридом натрия. Водород присоединяется по связи C=O. Реакция идет труднее, чем гидрирование алкенов: требуется нагревание, высокое давление и металлический катализатор (Pt,Ni
Среди кислородсодержащих органических соединений огромное значение имеют целых два класса веществ, которые всегда изучают вместе за схожесть в строении и проявляемых свойствах. Это альдегиды и кетоны. Именно эти молекулы лежат в основе многих химических синтезов, а их строение достаточно интересное, чтобы стать предметом изучения. Рассмотрим подробнее, что же представляют собой эти классы соединений.
Альдегиды и кетоны: общая характеристика
С точки зрения химии, к классу альдегидов следует относить органические молекулы, содержащие кислород в составе функциональной группы -СОН, называемой карбонильной. Общая формула в этом случае будет выглядеть так: R-COH. По своей природе это могут быть как предельные, так и непредельные соединения. Также среди них встречаются и ароматические представители, наравне с алифатическими. Количество атомов углерода в радикальной цепи варьируется в достаточно широких пределах, от одного (формальдегид или метаналь) до нескольких десятков.
Кетоны также содержат карбонильную группу -СО, однако соединена она не с катионом водорода, а с другим радикалом, отличным или идентичным тому, что входит в цепь. Общая формула выглядит так: R-CO-R , . Очевидно, что альдегиды и кетоны схожи по наличию функциональной группы такого состава.
Кетоны также могут быть предельными и непредельными, да и проявляемые свойства сходны с близкородственным классом. Можно привести несколько примеров, иллюстрирующих состав молекул и отражающих принятые обозначения формул рассматриваемых веществ.
- Альдегиды: метаналь - НСОН, бутаналь - СН 3 -СН 2 -СН 2 -СОН, фенилуксусный - С 6 Н 5 -СН 2 -СОН.
- Кетоны: ацетон или диметилкетон - СН 3 -СО-СН 3 , метилэтилкетон - СН 3 -СО-С 2 Н 5 и другие.
Очевидно, что название данных соединений образуется двумя путями:
- по рациональной номенклатуре согласно входящим в состав радикалам и классового суффикса -аль (для альдегидов) и -он (для кетонов);
- тривиально, исторически сложившееся.
Если привести общую формулу для обоих классов веществ, то станет видно, что они являются изомерами друг другу: C n H 2n O. Для них же самих характерны следующие виды изомерии:

Чтобы различать между собой представителей обоих классов, используют качественные реакции, большинство из которых позволяют выявить именно альдегид. Так как химическая активность данных веществ несколько выше, благодаря наличию катиона водорода.
Строение молекулы
Рассмотрим, как же в пространстве выглядят альдегиды и кетоны. Строение их молекул можно отразить несколькими пунктами.
- Атом углерода, непосредственно входящий в функциональную группу, имеет sp 2 - гибридизацию, что позволяет части молекулы иметь плоскую пространственную форму.
- При этом полярность связи С=О сильна. Как более электроотрицательный, кислород забирает себе основную часть плотности, концентрируя на себе частично отрицательный заряд.
- В альдегидах связь О-Н является также сильно поляризованной, что делает атом водорода подвижным.
В результате получается, что подобное строение молекул позволяет рассматриваемым соединениям и окисляться, и восстанавливаться. Формула альдегида и кетона с перераспределенной электронной плотностью позволяет предсказать продукты реакций, в которых участвуют данные вещества.
История открытия и изучения
Как и многие органические соединения, выделить и изучить альдегиды и кетоны людям удалось лишь в XIX веке, когда виталистические взгляды полностью рухнули и стало понятно, что эти соединения могут образовываться синтетическим, искусственным путем, без участия живых существ.
Однако еще в 1661 году Р. Бойль сумел получить ацетон (диметилкетон), когда подвергал нагреванию ацетат кальция. Но подробно изучить это вещество и назвать его, определить систематическое положение среди других, он не смог. Лишь в 1852 году Уильямсон сумел довести это дело до конца, тогда и началась история подробного развития и накопления знаний о карбонильных соединениях.

Физические свойства
Рассмотрим, каковы физические свойства альдегидов и кетонов. Начнем с первых.
- Первый представитель метаналь по агрегатному состоянию - газ, следующие одиннадцать - жидкости, свыше 12 атомов углерода входят в состав твердых альдегидов нормального строения.
- Температура кипения: зависит от числа атомов С, чем их больше, тем она выше. При этом чем более разветвлена цепочка, тем ниже опускается значение температуры.
- Для жидких альдегидов показатели вязкости, плотности, преломления зависят также от числа атомов. Чем их больше, тем они выше.
- Газообразный и жидкие альдегиды растворяются в воде очень хорошо, однако твердые практически не могут этого делать.
- Запах представителей очень приятный, часто это ароматы цветов, духов, фруктов. Лишь те альдегиды, в которых количество атомов углерода равно 1-5, являются сильно и неприятно пахнущими жидкостями.
Если обозначать свойства кетонов, то также можно выделить главные.
- Агрегатные состояния: низшие представители - жидкости, более массивные - твердые соединения.
- Запах резкий, неприятный у всех представителей.
- Растворимость в воде хорошая у низших, в органических растворителях отличная у всех.
- Летучие вещества, данный показатель превышает таковой у кислот, спиртов.
- Температура кипения и плавления зависит от строения молекулы, сильно варьируется от количества атомов углерода в цепи.
Это основные свойства рассматриваемых соединений, которые относятся к группе физических.

Химические свойства
Самое важное, это с чем реагируют альдегиды и кетоны, химические свойства данных соединений. Поэтому их мы рассмотрим обязательно. Сначала разберемся с альдегидами.
- Окисление до соответствующих карбоновых кислот. Общий вид уравнения реакции: R-COH + [O] = R-COOH. Ароматические представители еще легче вступают в подобные взаимодействия, также они способны формировать в результате сложные эфиры, имеющие важное промышленное значение. В качестве окислителей используют: кислород, реактив Толленса, гидроксид меди (II) и другие.
- Альдегиды проявляют себя как сильные восстановители, при этом превращаясь в предельные одноатомные спирты.
- Взаимодействие со спиртами с образованием продуктов ацеталей и полуацеталей.
- Особые реакции - поликонденсации. В результате образуются фенолформальдегидные смолы, имеющие значение для химической промышленности.
- Несколько специфических реакций со следующими реактивами:
- водно-спиртовая щелочь;
- реактив Гриньяра;
- гидросульфиты и прочие.
Качественной реакцией на данный класс веществ является реакция "серебряного зеркала". В результате нее образуется металлическое восстановленное серебро и соответствующая карбоновая кислота. Для нее необходим аммиачный раствор оксида серебра или реактив Толлинса.

Химические свойства кетонов
Спирты, альдегиды, кетоны являются схожими по проявляемым свойствам соединениями, так как все они кислородсодержащие. Однако уже на стадии окисления становится ясно, что спирты - самые активные и легко поддающиеся воздействию соединения. Кетоны же окислить труднее всего.
- Окислительные свойства. В результате образуются вторичные спирты.
- Гидрирование также приводит к упомянутым выше продуктам.
- Кето-енольная таутомерия - особое специфическое свойство кетонов принимать бета-форму.
- Реакции альдольной конденсации с образование бета-кетоспиртов.
- Также кетоны способны взаимодействовать с:
- аммиаком;
- синильной кислотой;
- гидросульфитами;
- гидразином;
- ортокремниевой кислотой.
Очевидно, что реакции таких взаимодействий очень сложны, особенно те, которые являются специфическими. Это все основные особенности, которые проявляют альдегиды и кетоны. Химические свойства лежат в основе многих синтезов важных соединений. Поэтому знать природу молекул и их характер при взаимодействиях крайне необходимо в промышленных процессах.
Реакции присоединения альдегидов и кетонов
Мы уже рассмотрели данные реакции, однако не давали им такого названия. К присоединению можно отнести все взаимодействия, в результате которых активность проявила карбонильная группа. А точнее, подвижный атом водорода. Именно поэтому в данном вопросе преимущество отдается именно альдегидам, вследствие их лучшей реакционноспособности.
С какими веществами возможны реакции альдегидов и кетонов по нуклеофильному замещению? Это:
- Синильная кислота, образуются циангидрины - исходное сырье при синтезе аминокислот.
- Аммиак, амины.
- Спирты.
- Воду.
- Гидросульфат натрия.
- Реактив Гриньяра.
- Тиолы и другие.
Эти реакции имеют важное промышленное значение, поскольку продукты используются в разных областях жизнедеятельности людей.

Способы получения
Существует несколько основных методов, которыми синтезируют альдегиды и кетоны. Получение в лаборатории и промышленности можно выразить в следующих способах.
- Самым распространенным методом, в том числе и в лабораториях, является окисление соответствующих спиртов: первичных до альдегидов, вторичных до представителей кетонов. В качестве окислительного агента могут выступать: хроматы, ионы меди, перманганат калия. Общий вид реакции: R-OH + Cu (KMnO 4) = R-COH.
- В промышленности часто используют способ, основанный на окислении алкенов - оксосинтез. Основной агент синтез-газ, смесь СО 2 + Н 2 . Результатом становится альдегид с большим на один углерод числом атомов в цепи. R=R-R + СО 2 + Н 2 = R-R-R-COH.
- Окисление алкенов озоном - озонолиз. Результат также предполагает альдегид, но кроме этого еще и кетон в смеси. Если продукты мысленно соединить, убрав кислород, станет ясно, какой исходный алкен был взят.
- Реакция Кучерова - гидратация алкинов. Обязательный агент - соли ртути. Один из промышленных способов синтеза альдегидов и кетонов. R≡R-R + Hg 2+ + H 2 O = R-R-COH.
- Гидролиз дигалогенпроизводных углеводородов.
- Восстановление: карбоновых кислот, амидов, нитрилов, хлорангидридов, сложных эфиров. В результате образуется как альдегид, так и кетон.
- Пиролиз смесей карбоновых кислот над катализаторами в виде оксидов металлов. Смесь должна быть парообразной. Суть заключается в отщеплении между молекулами диоксида углерода и воды. В результате образуется альдегид или кетон.
Ароматические альдегиды и кетоны получают иными способами, так как данные соединения имеют ароматический радикал (фенил, например).
- По Фриделю-Крафтсу: в исходных реагентах ароматический углеводород и дигалогензамещенный кетон. Катализатор - ALCL 3 . В результате образуется ароматический альдегид или кетон. Другое название процесса - ацилирование.
- Окисление толуола действием разных агентов.
- Восстановлением ароматических карбоновых кислот.
Естественно, что в промышленности стараются использовать те методы, в которых исходное сырье как можно более дешевое, а катализаторы менее токсичные. Для синтеза альдегидов - это окисление алкенов кислородом.

Применение в промышленности и значение
Применение альдегидов и кетонов осуществляется в таких отраслях промышленности, как:
- фармацевтика;
- химический синтез;
- медицина;
- парфюмерная область;
- пищевая промышленность;
- лакокрасочное производство;
- синтез пластмасс, тканей и прочее.
Можно обозначить еще не одну область, ведь ежегодно только формальдегида синтезируется приблизительно 6 млн т в год! Его 40% раствор именуется формалином и используется для хранения анатомических объектов. Он же идет на изготовление лекарственных препаратов, антисептиков и полимеров.
Уксусный альдегид, или этаналь, также массово производимый продукт. Количество ежегодного потребления в мире составляет около 4 млн т. Он - основа многих химических синтезов, при которых образуются важные продукты. Например:
- уксусная кислота и ее ангидрид;
- ацетат целлюлозы;
- лекарства;
- бутадиен - основа каучука;
- ацетатное волокно.
Ароматические альдегиды и кетоны - это составная часть многих ароматизаторов, как пищевых, так и парфюмерных. Большинство из них имеют очень приятные цветочные, цитрусовые, травяные ароматы. Это позволяет изготовлять на их основе:
- освежители воздуха различного рода;
- туалетные и парфюмерные воды;
- различные чистящие и моющие средства.
Некоторые из них являются ароматическими добавками к пище, разрешенными к употреблению. Их природное содержание в эфирных маслах, фруктах и смолах доказывают возможность подобного использования.
Отдельные представители
Такой альдегид, как цитраль, представляет собой жидкость с большой вязкостью и сильным ароматом лимона. В природе содержится как раз в эфирных маслах последнего. Также в составе эвкалипта, сорго, кебаба.
Хорошо известны области его применения:
- педиатрия - понижение внутричерепного давления;
- нормализация артериального давления у взрослых;
- компонент лекарства для органов зрения;
- составная часть многих душистых веществ;
- противовоспалительное средство и антисептик;
- сырье для синтеза ретинола;
- ароматизатор в пищевых целях.
(для простейшего альдегида R=H)
Классификация альдегидов
По строению углеводородного радикала:
Предельные; например:

Непредельные; например:

Ароматические; например:

Алициклические; например:

Общая формула предельных альдегидов

Гомологический ряд, изомерия, номенклатура

Альдегиды изомерны другому классу соединений - кетонам

например:

Альдегиды и кетоны содержат карбонильную группу ˃C=O, поэтому называются карбонильными соединениями.
Электронное строение молекул альдегидов
Атом углерода альдегидной группы находится в состоянии sp 2 -гибридизации, поэтому все σ-связи в этой группе располагаются в одной плоскости. Облака р-электронов, образующих π-связь, перпендикулярны этой плоскости и легко смещаются к более электроотрицательному атому кислорода. Поэтому двойная связь C=O (в отличие от двойной связи C=C в алкенах) сильно поляризована.
Физические свойства

Химические свойства
Альдегиды - реакционноспособные соединения, вступающие в многочисленные реакции. Наиболее характерны для альдегидов:
а) реакции присоединения по карбонильной группе; реагенты типа НХ присоединяются следующим образом:

б) реакции окисления связи C-H альдегидной группы, в результате которых образуются карбоновые кислоты:
I. Реакции присоединения
1. Гидрирование (образуются первичные спирты

2. Присоединение спиртов (образуются полуацетали и ацетали)

В избытке спирта в присутствии HCl полуацетали превращаются в ацетали:

II. Реакции окисления
1. Реакция «серебряного зеркала»

Упрощённо:

Эта реакция является качественной реакцией на альдегидную группу (на стенках реакционного сосуда образуется зеркальный налет металлического серебра).
2. Реакция с гидроксидом меди (II)

Эта реакция также является качественной реакцией на альдегидную групп у (выпадает красный осадок Сu 2 O).
Формальдегид окисляется различными O-содержащими окислителями сначала до муравьиной кислоты и далее - до Н 2 СO 3 (СO 2 + Н 2 O):

III. Реакции ди-, три- и полимеризации
1. Альдольная конденсация

2. Тримеризация ацетальдегида

3. Полимеризация формальдегида
При длительном хранении формалина (40%-ный водный раствор формальдегида) в нем происходит полимеризация с образованием белого осадка параформа:

IV. Реакция поликонденсации формальдегида с фенолом

Первая группа свойств реакции присоединения. В карбонильной группе между углеродом и кислородом присутствует двойная связь, которая, как вы помните, состоит из сигма-связи и пи-связи. В реакциях присоединения пи-связь рвется и образуются две сигма связи одна с углеродом, вторая с кислородом. На углероде сосредоточен частичный положительный заряд, на кислороде частичный отрицательный. Поэтому к углероду присоединяется отрицательно заряженная частица реагента, анион, а к кислород положительно заряженная часть молекулы.
Первое свойство гидрирование, присоединение водорода.
Реакция проходит при нагревании. Применяется уже известный вам катализатор гидрирования никель. Из альдегидов получаются первичные спирты, из кетонов вторичные.

У вторичных спиртов гидроксогруппа связана со вторичным атомом углерода.
Второе свойство гидратация, присоединение воды. Эта реакция возможна только для формальдегида и ацетальдегида. Кетоны совсем не реагируют с водой.
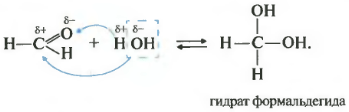
Все реакции присоединения идут таким образом, что плюс идет к минусу, а минус к плюсу.
Как вы помните из видео про спирты , наличие двух гидроксогрупп у одного атома почти невозможная ситуация, такие вещества крайне неустойчивы. Так вот конкретно два этих случая гидрат формальдегида и уксусного альдегида возможны, хотя и существуют только в растворе.
Сами реакции знать не обязательно. Скорее всего, вопрос на экзамене может звучать как констатация факта, допустим, с водой реагируют и перечислены вещества. Среди их перечня которых могут быть метаналь или этаналь.
Третье свойство присоединение синильной кислоты.

Снова плюс идет к минусу, а минус к плюсу. Получаются вещества, называемые гидроксинитрилами. Опять же, сама реакция встречается нечасто, но знать об этом свойстве нужно.
Четвертое свойство присоединение спиртов.
Здесь снова не нужно знать наизусть уравнение реакции, просто надо понимать, что такое взаимодействие возможно.

Как обычно в реакциях присоединения к карбонильной группе плюс к минусу, а минус к плюсу.
Пятое свойство реакция с гидросульфитом натрия.

И снова, реакция довольно сложная, выучить ее вряд ли получится, но это одна из качественных реакций на альдегиды, потому что полученная натриевая соль выпадает в осадок. То есть по факту вы должны знать, что альдегиды реагируют с гидросульфитом натрия, этого будет достаточно.
На этом закончим с первой группой реакций. Вторая группа реакции полимеризации и поликонденсации.
2. Полимеризация и поликонденсация альдегидов
С полимеризацией вы знакомы: полиэтилен, бутадиеновый и изопреновый каучуки, поливинилхлорид это продукты объединения множества молекул (мономеров) в одну большую, в единую полимерную цепь. То есть получается один продукт. При поликонденсации происходит то же самое, но помимо полимера получаются еще низкомолекулярные продукты, например, вода. То есть получается два продукта.
Итак, шестое свойство полимеризация. Кетоны в эти реакции не вступают, промышленное значение имеет только полимеризация формальдегида.
Пи-связь рвется и образуются две сигма связи с соседними мономерами. Получается полиформальдегид, называемый также параформ. Вероятнее всего, вопрос на экзамене может звучать так: в реакции полимеризации вступают вещества. И приведен список веществ, среди которых может быть в формальдегид.
Седьмое свойство поликонденсация. Еще раз: при поликонденсации помимо полимера получается еще низкомолекулярное соединение, например, вода. Формальдегид вступает в такую реакцию с фенолом. Для наглядности сначала запишем уравнение с двумя молекулами фенола.

В результате получается такой димер и отщепляется молекула воды. Теперь запишем уравнение реакции в общем виде.

Продуктом поликонденсации является феноло-формальдегидная смола. Она находит широкое применение от клеев и лаков до пластмасс и компонента древесно-стружечных плит.
Теперь третья группа свойств реакции окисления.
3. Окисление альдегидов и кетонов
Восьмой реакцией в общем списке является качественная реакция на альдегидную группу окисление аммиачным раствором оксида серебра. Реакция «серебряного зеркала». Скажу сразу, кетоны не вступают в эту реакцию, только альдегиды.

Альдегидная группа окисляется до карбоксильной, кислотной группы, но в присутствии аммиака, который является основание, сразу же происходит реакция нейтрализации и получается соль ацетат аммония. Серебро выпадает в осадок, покрывая пробирку изнутри и создавая зеркальную поверхность. Эта реакция встречается на ЕГЭ постоянно.
Кстати, эта же реакция является качественной на другие вещества, имеющие альдегидную группу, например, на муравьиную кислоту и ее соли, а также на глюкозу.
Девятая реакция тоже качественная на альдегидную группу окисление свежеосажденным гидроксидом меди два. Здесь тоже замечу, что кетоны не вступают в эту реакцию.

Визуально будет наблюдаться сначала образование желтого осадка, который потом становится красным. В некоторых учебниках встречается информация, что сначала образуется гидроксид меди один, имеющий желтый цвет, который затем распадается на красный оксид меди один и воду. Так вот это неверно по последним данным в процессе выпадения осадка меняется размер частиц оксида меди один, которые в конечном счете достигают размеров, окрашенных именно в красный цвет. Альдегид окисляется до соответствующей карбоновой кислоты. Реакция встречается на егэ очень часто.
Десятая реакция окисление альдегидов подкисленным раствором перманганата калия при нагревании.
Происходит обесцвечивание раствора. Альдегидная группа окисляется до карбоксильной, то есть альдегид окисляется до соответствующей кислоты. Для кетонов эта реакция не имеет практического смысла, поскольку происходит разрушение молекулы и в результате получается смесь продуктов.
Важно отметить, что муравьиный альдегид, формальдегид, окисляется до углекислого газа, потому как соответствующая ему муравьиная кислота сама не устойчива к действию сильных окислителей.
В итоге углерод переходит из степени окисления 0 в степень окисления +4. Напомню, что и метанол, как правило, в таких условиях окисляется по максимуму до CO 2 , проскакивая стадию и альдегида, и кислоты. Эту особенность надо запомнить.
Одиннадцатая реакция горение, полное окисление. И альдегиды, и кетоны сгорают до углекислого газа и воды.
Запишем уравнение реакции в общем виде.
По закону сохранения массы атомов слева должно быть столько же, сколько атомов справа. Потому что ведь в химических реакциях атомы никуда не деваются, а просто изменяется порядок связей между ними. Так вот молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле карбонильного соединения, поскольку в состав молекулы входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть 2n/2, а значит просто n.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа, потому что в каждой молекуле два атома кислорода, плюс n воды, итого 3n. Слева атомов кислорода столько же 3n, но один из атомов находится в молекуле альдегида, значит его надо вычесть из общего количества, чтобы получить количество атомов, приходящихся на молекулярный кислород. Выходит 3n-1 атомов содержит молекулярный кислород, а значит молекул в 2 раза меньше, потому как в состав одной молекулы входят 2 атома. То есть (3n-1)/2 молекул кислорода.
Таким образом, мы составили уравнение сгорания карбонильных соединений в общем виде.
И, наконец, двенадцатое свойство, относящееся к реакциям замещения галогенирование по альфа-атому углерода. Еще раз обратимся к строению молекулы альдегида. Кислород оттягивает на себя электронную плотность, создавая частичный положительный заряд а углероде. Метильная группа пытается компенсировать этот положительный заряд, смещая к нему электроны от водорода по цепи сигма-связей. Связь углерод-водород становится более полярной и водород легче отрывается при атаке реагентом. Такой эффект наблюдается только для альфа-атома углерода, то есть атома следующего за альдегидной группой, вне зависимости от длины углеводородного радикала.
Таким образом, возможно получение, например, 2-хлорацетальдегида. Возможно дальнейшее замещение атомов водорода до трихлорэтаналя.
Вопрос 1. Альдегиды. Их строение, свойства, получение и применение.
Ответ. Альдегиды – органические вещества, молекулы которых
Общая формула альдегидов ˸
Номенклатура
Наименование альдегидов производят от исторических названий карбоновых кислот с тем же числом атомов углерода. Так, CH 3 CHO – уксусный альдегид. По систематической номенклатуре название альдегидов производят от названий углеводородов с прибавлением окончания –аль , CH 3 CHO – этаналь. Нумерацию углеродной цепи начинают с карбонильной группы. Для разветвленных изомеров перед названием альдегида записывают названия заместителей с указанием цифрой и номера углеродного атома, с которым они связаны˸
CH 3 – CH (CH 3) – CH 2 – CHO.
3-метилбутаналь
Изомерия
Углеродного скелета ˸
CH 3 – CH 2 – CH 2 – CHO – бутаналь,
CH 3 – CH(CH 3) – CHO – 2-метилпропаналь.
Классов соединений ˸
CH 3 – CH 2 – CHO – пропаналь,
CH 3 – CO – CH 3 – пропанон (ацетон).
Физические свойства
Метаналь – газ, альдегид от C 2 до С 13 – жидкости, высшее альдегиды – твердые вещества (тетрадеканаль или миристиновый альдегид CH 3 (CH 2) 12 CHO имеет температуру плавления 23,5 ). Низшие альдегиды хорошо растворимы в воде; чем больше атомов углерода в молекуле, тем меньше растворимость; у альдегидов нет водородной связей.
Химические свойства
1. Реакции присоединения ˸
а) гидрирование ˸
CH 2 O + H 2 = CH 3 OH;
б) образование ацеталий со спиртами ˸
CH 3 - CH 2 – CHO + 2C 2 H 5 OH = CH 3 – CH 2 – CH(OC 2 H 5) 2 + H 2 O.
2. Реакция окисления˸
а) реакция ʼʼсеребряного зеркалаʼʼ ˸
CH 3 CHO + Ag 2 O 2 Ag + CH 3 COOH;
б) взаимодействие с гидрооксидом меди (II) ˸
CH 3 CHO + 2Cu(OH) 2 CH 3 COOH + Cu 2 O↓ + 2H 2 O
3. Реакции замещения˸
CH 3 CH 2 CHO + Br 2 = CH 3 – CH (Br) – CHO+ HBr
4.Полимеризация˸
CH3=O (CH 2 O) 3 .
триоксиметилен
5.Поликонденсация˸
n C 6 H 5 OH + n CH 2 O + n C 6 H 5 OH + …=
=[ C 6 H 4 (OH) – CH 2 – C 6 H 4 (OH)] n + n H 2 O
Фенолформальдегидная смола
Получение
а) Окисление алканов˸
CH 4 + O 2 CH 2 O + H 2 O.
метаналь
б) Окисление спиртов˸
2CH 3 OH + O 2 2CH 2 O + 2H 2 O.
в) Реакция Кучерова˸
C 2 H 2 + H 2 O CH 3 CHO.
г) Окисление алкенов˸
C 2 H 4 + [O] CH 3 CHO.
Применение˸
1. Получение фенолформальдегидных смол, пластмасс.
2. Производство лекарств, формалина (из CH 2 =O).
3. Производство красителей.
4. Производство уксусной кислоты.
5. Дезинфекция и протравливание семян.
Вопрос 2. Проблема защита окружающей среды .
Ответ ˸ На сегодняшний день самым крупномасштабным является загрязнение окружающей среды химическими веществами.
Охрана атмосферы
Источники загрязнения˸ предприятия чёрной и цветной металлургии, теплоэлектростанции, автотранспорт.
Промышленность˸ выбросы оксидов серы и азота. В результате обжига сульфидных руд цветных металлов выделяется оксид серы (IV).
Теплоэлектростанции выделяют SO 2 и SO 3 ,которые соединяются с влагой воздуха (SO 3 + H 2 O = H 2 SO 4)и выпадают с виде кислотных дождей.
Вопрос 1. Альдегиды. Их строение, свойства, получение и применение. - понятие и виды. Классификация и особенности категории "Вопрос 1. Альдегиды. Их строение, свойства, получение и применение." 2015, 2017-2018.









