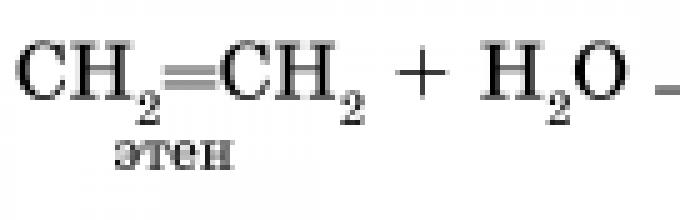В материале рассмотрена класиификация кислородсодержащих органических веществ. Разобрны вопросы гомологии, изомерии и номенклатуры веществ. Презнтация насыщена заданиями по данным вопросам. Закрепление материала предлагается в тестового упражнения на соответствие.
Скачать:
Предварительный просмотр:
Чтобы пользоваться предварительным просмотром презентаций создайте себе аккаунт (учетную запись) Google и войдите в него: https://accounts.google.com
Подписи к слайдам:
Задачи урока: познакомиться с классификацией кислородсодержащих органических соединений; построение гомологических рядов веществ; выявление возможных видов изомерии; построение структурных формул изомеров веществ, номенклатура веществ.
Классификация веществ С х Н у О z карбоновые кислоты альдегиды кетоны эфиры спирты фенолы одно- атомные -много R – OH R–(OH) n простые сложные OH = R – C - O OH = R – C - O H - овая кислота -аль R – C – R || O -он R – O – R = R – C - O O – R - ол - n ол
Гомологический ряд СН 3 – ОН С 2 Н 5 – ОН С 3 Н 7 – ОН С 4 Н 9 – ОН С 5 Н 11 – ОН метан ол этан ол пропан ол-1 бутан ол-1 пентан ол-1 Спирты С n H 2n+2 O
Карбоновые кислоты = Н – C - O OH = СН 3 – C - O OH = СН 3 – СН 2 – C - O OH метан овая кислота (муравьиная) этан овая кислота (уксусная) пропан овая кислота (пропионовая) С n H 2n O 2
Альдегиды = Н – C - O H = СН 3 – C - O H = СН 3 – СН 2 – C - O H метан аль муравьиный альдегид (формальдегид) этан аль уксусный альдегид (ацетальдегид) пропан аль пропионовый альдегид С n H 2n O
Кетоны СН 3 – C – СН 3 || O СН 3 – СН 2 – C – СН 3 || O СН 3 – СН 2 – СН 2 – C – СН 3 || O пропан он (ацетон) бутан он пентан он-2 С n H 2n O
Простые эфиры СН 3 – О –СН 3 С 2 Н 5 – О –СН 3 С 2 Н 5 – О –С 2 Н 5 С 3 Н 7 – О –С 2 Н 5 С 3 Н 7 – О –С 3 Н 7 диметил овый эфир метиэтил овый эфир диэтил овый эфир этилпропил овый эфир дипропил овый эфир С n H 2n+2 O Вывод: простые эфиры – производные предельных одноатомных спиртов.
Сложные эфиры = Н – C - O O – СН 3 = СН 3 – C - O O – С Н 3 = СН 3 – СН 2 – C - O O – СН 3 метиловый эфир муравьиной кислоты (метил формиат) метиловый эфир уксусной кислоты (метил ацетат) метиловый эфир пропионовой кислоты С n H 2n O 2 Вывод: сложные эфиры – производные карбоновых кислот и спиртов.
спирты эфиры кетоны альдегиды карбоновые кислоты Изомерия и номенклатура изомерия углеродного скелета межклассовая (сложные эфиры) углеродного скелета межклассовая (кетоны) углеродного скелета положения f- группы (-С =О) межклассовая (альдегиды) углеродного скелета положения f- группы (-ОН) межклассовая (простые эфиры) углеродного скелета межклассовая
Составление формул изомеров. Номенклатура веществ. Задание: составьте структурные формулы возможных изомеров для веществ состава С 4 Н 10 О; С 4 Н 8 О 2 ; С 4 Н 8 О. К каким классам они принадлежат? Назовите все вещества по систематической номенклатуре. С 4 Н 10 О С 4 Н 8 О 2 С 4 Н 8 О С n H 2n+2 O С n H 2n O 2 С n H 2n O спирты и простые эфиры карбоновые кислоты и сложные эфиры альдегиды и кетоны
СН 3 – СН 2 – СН – СН 3 | ОН СН 3 | СН 3 – С – СН 3 | ОН СН 3 – О – СН 2 – СН 2 – СН 3 СН 3 – СН 2 – О – СН 2 – СН 3 бутанол-1 2-метилпропанол-1 бутанол-2 2-метилпропанол-2 метилпропиловый эфир диэтиловый эфир I спирты II спирт III спирт
СН 3 – СН 2 – СН 2 – C - O OH = СН 3 – СН – C - O OH | СН3 = СН 3 – СН 2 – C - O O – СН 3 = СН 3 – C - O O – СН 2 – СН 3 бутановая кислота 2-метилпропановая кислота метиловый эфир пропионовой к-ты этиловый эфир уксусной кислоты
СН 3 – СН 2 – СН 2 – C - O H = СН 3 – СН – C - O H | СН3 СН 3 – СН 2 – C – СН 3 || O бутаналь 2-метилпропаналь бутанон-2
Проверь себя! 1. Установите соответствие: общая формула класс вещество R – COOH R – O – R R – COH R – OH R – COOR 1 R – C – R || O сл. эфиры спирты карб. к-ты кетоны альдегиды пр. эфиры а) С 5 Н 11 –ОН б) С 6 Н 13 –СОН в) С 4 Н 9 –О–СН 3 г) С 5 Н 11 –СООН д) СН 3 –СО–СН 3 е) СН 3 –СООС 2 Н 5 2. Назовите вещества по систематической номенклатуре.
Проверь себя! I II III IV V VI 3 6 5 2 1 4 Г В Б А Е Д
Домашнее задание Параграф (17-21) – 1 и 2 части упр. 1,2,4,5 стр. 153-154 2 стр. 174 Урок окончен!
Образование галогеналканов при взаимодействии спиртов с галогеноводородами - обратимая реакция. Поэтому понятно, что спирты могут быть получены при гидролизе галогеналканов - реакции этих соединений с водой:
Многоатомные спирты можно получить при гидролизе галогеналканов, содержащих более одного атома галогена в молекуле. Например:
Гидратация алкенов
Гидратация алкенов - присоединение воды по π — связи молекулы алкена, например:
![]()
Гидратация пропена приводит в соответствии с правилом Марковникова к образованию вторичного спирта - пропанола-2:

Гидрирование альдегидов и кетонов
Окисление спиртов в мягких условиях приводит к образованию альдегидов или кетонов. Очевидно, что спирты могут быть получены при гидрировании (восстановлении водородом, присоединении водорода) альдегидов и кетонов:

Окисление алкенов
Гликоли, как уже отмечалось, могут быть получены при окислении алкенов водным раствором перманганата калия. Например, этиленгликоль (этандиол-1,2) образуется при окислении этилена (этена):
Специфические способы получения спиртов
1. Некоторые спирты получают характерными только для них способами. Так, метанол в промышленности получают реакцией взаимодействия водорода с оксидом углерода (II) (угарным газом) при повышенном давлении и высокой температуре на поверхности катализатора (оксида цинка):
![]()
Необходимую для этой реакции смесь угарного газа и водорода, называемую также «синтез-газ», получают при пропускании паров воды над раскаленным углем:
![]()
2. Брожение глюкозы . Этот способ получения этилового (винного) спирта известен человеку с древнейших времен:
![]()
Основными способами получения кислородсодержащих соединений (спиртов) являются: гидролиз галогеналканов, гидратация алкенов, гидрирование альдегидов и кетонов, окисление алкенов, а также получение метанола из «синтез-газа» и сбраживание сахаристых веществ.
Способы получения альдегидов и кетонов
1. Альдегиды и кетоны могут быть получены окислением или дегидрированием спиртов . При окислении или дегидрировании первичных спиртов могут быть получены альдегиды, а вторичных спиртов - кетоны:
 3CH 3 –CH 2 OH + K 2 Cr 2 O 7 + 4H 2 SO 4 = 3CH 3 –CHO + K 2 SO 4 + Cr 2 (SO 4) 3 + 7H 2 O
3CH 3 –CH 2 OH + K 2 Cr 2 O 7 + 4H 2 SO 4 = 3CH 3 –CHO + K 2 SO 4 + Cr 2 (SO 4) 3 + 7H 2 O
2. Реакция Кучерова. Из ацетилена в результате реакции получается уксусный альдегид, из гомологов ацетилена - кетоны:

3. При нагревании кальциевых или бариевых солей карбоновых кислот образуются кетон и карбонат металла:

Способы получения карбоновых кислот
1. Карбоновые кислоты могут быть получены окислением первичных спиртов или альдегидов :
 3CH 3 –CH 2 OH + 2K 2 Cr 2 O 7 + 8H 2 SO 4 = 3CH 3 –COOH + 2K 2 SO 4 + 2Cr 2 (SO 4) 3 + 11H 2 O
3CH 3 –CH 2 OH + 2K 2 Cr 2 O 7 + 8H 2 SO 4 = 3CH 3 –COOH + 2K 2 SO 4 + 2Cr 2 (SO 4) 3 + 11H 2 O
5CH 3 –CHO + 2KMnO 4 + 3H 2 SO 4 =5CH 3 –COOH + 2MnSO 4 + K 2 SO 4 + 3H 2 O,
3CH 3 –CHO + K 2 Cr 2 O 7 + 4H 2 SO 4 = 3CH 3 –COOH + Cr 2 (SO 4) 3 + K 2 SO 4 + 4H 2 O,
CH 3 –CHO + 2OH CH 3 –COONH 4 + 2Ag + 3NH 3 + H 2 O.
Но при окислении метаналя аммиачным раствором оксида серебра, образуется карбонат аммония, а не муравьиная кислота:
HCHО + 4OH = (NH 4) 2 CO 3 + 4Ag + 6NH 3 + 2H 2 O.
2. Ароматические карбоновые кислоты образуются при окислении гомологов бензола :

5C 6 H 5 –CH 3 + 6KMnO 4 + 9H 2 SO 4 = 5C 6 H 5 COOH + 6MnSO 4 + 3K 2 SO 4 + 14H 2 O,
5C 6 H 5 –C 2 H 5 + 12KMnO 4 + 18H 2 SO 4 = 5C 6 H 5 COOH + 5CO 2 + 12MnSO 4 + 6K 2 SO 4 + 28H 2 O,
C 6 H 5 –CH 3 + 2KMnO 4 = C 6 H 5 COOK + 2MnO 2 + KOH + H 2 O
3. Гидролиз различных производных карбоновых кислот также приводит к получению кислот. Так, при гидролизе сложного эфира образуются спирт и карбоновая кислота. Реакции этерификации и гидролиза, катализируемой кислотой, обратимы:
4. Гидролиз сложного эфира под действием водного раствора щелочи протекает необратимо, в этом случае из сложного эфира образуется не кислота, а ее соль:
Цели. Познакомить с большой группой органических веществ, генетически связанных между собой (строением, изомерией, номенклатурой, физическими свойствами, классификацией); сформировать общее представление о спиртах, альдегидах, карбоновых кислотах; продолжить развитие общеучебных навыков; воспитывать потребности в знаниях о тех веществах, с которыми мы соприкасаемся в быту – они находятся в пищевых продуктах, лекарствах.
Демонстрационный материал. Коллекция карбоновых кислот, спиртов, фенола, формалина.
Демонстрационный эксперимент. Изучение растворимости в воде спиртов (этанола, н -пропанола и н -бутанола), кислот (муравьиной, уксусной, пропионовой, масляной, стеариновой и пальмитиновой), альдегидов (40%-й раствор муравьиного альдегида – формалин).
Наглядное обеспечение. Таблицы «Образование водородной связи», «Спирты и альдегиды»; модели молекул; рисунки с формулами наиболее часто встречаемых кислот.
Раздаточный материал. Информационная карта к занятию.
Межпредметные и внутрипредметные связи. Неорганическая химия: минеральные кислоты, водородные связи между молекулами; органическая химия: углеводороды (общие формулы, строение, номенклатура, изомерия); математика: функция; физика: физические свойства веществ, константы.
ХОД УРОКА
П р и м е р ы: муравьиная кислота, щавелевая кислота, лимонная, яблочная, молочная кислоты, «винный спирт» (этанол), формалин (40%-й раствор муравьиного альдегида в воде), глицерин, ацетон, эфир для наркоза (диэтиловый эфир), фенол.
Задание 1. Распределите следующие вещества на три группы – спирты, альдегиды, карбоновые кислоты:

Задание 2. По каким признакам классифицируют кислородсодержащие соединения? Назовите функциональные группы спиртов, альдегидов и карбоновых кислот.
Функциональные группы веществ разных классов
СпиртыАльдегиды
Карбоновые кислоты
ОН
гидроксильная
Задание 3. Как называют углеводородный фрагмент в формулах органических кислородсодержащих соединений? Например, в задании 1 (см. выше) – это фрагменты: СН 3 , С 4 Н 9 , С 5 Н 11 , С 2 Н 5 , С 7 Н 15 , С 3 Н 7 .
Обозначая углеводородный радикал буквой R, получаем общие формулы:
спиртов – ………………………. ;
альдегидов – ……………….. ;
органических кислот – …………………. .
Классификацию спиртов, альдегидов и кислот можно проводить по числу функциональных групп в молекулах. Различают одно-, двух- и трехатомные спирты:

Альдегиды с двумя альдегидными группами СНО в молекуле называют следующим образом:

Карбоновые кислоты в зависимости от числа карбоксильных групп в молекуле бывают одно-, двух- и трехосновные:

Кислородсодержащие соединения различаются по строению углеводородного радикала. Они бывают предельные (насыщенные), непредельные (ненасыщенные), циклические, ароматические.
Примеры спиртов:

Примеры альдегидов:

Примеры карбоновых кислот:

Мы будем изучать только предельные одноосновые карбоновые кислоты, одноатомные спирты и альдегиды.
Задание 4. Дайте определение насыщенных спиртов, альдегидов, карбоновых кислот.
Спирты бывают первичные, вторичные и третичные. В первичных спиртах при атоме С, связанном с гидроксильной группой ОН, один углеродный сосед; во вторичных спиртах при атоме С наряду с группой ОН два углеродных заместителя (соседа), а в третичных спиртах – три углеродных заместителя. Например:

Номенклатура
кислородсодержащих соединений
По международной номенклатуре ИЮПАК названия спиртов производят из названий соответствующих алканов с добавлением суффикса «ол».
Задание 5. Напишите молекулярные формулы и названия четырех первичных спиртов с числом атомов углерода в молекуле 4 и более.Особенность названий альдегидов – суффикс «аль».
Задание 6. Впишите в таблицу формулы и названия по ИЮПАК следующих четырех альдегидов.
Задание 7. Впишите в таблицу формулы и названия по ИЮПАК четырех следующих кислот.
Задание 8. Почему метаналь и метановую кислоту нельзя считать гомологами? Чем они отличаются от гомологов?
Физические свойства.
Водородная связь
1) А г р е г а т н о е с о с т о я н и е линейных соединений разных классов.
Задание 9. Почему среди алканов так много газов? Почему существует газообразный альдегид при нормальных условиях (0 °С, 1 атм)? С чем это может быть связано?2) Т е м п е р а т у р ы к и п е н и я (°С) первых пяти гомологов веществ четырех классов.
Задание 10. Сравните температуры кипения соответствующих (по числу атомов С) алканов, спиртов, альдегидов и карбоновых кислот. Какие особенности этой характеристики у веществ разных гомологических рядов?3) В о д о р о д н а я с в я з ь в ряду рассматриваемых соединений – это межмолекулярная связь между кислородом одной молекулы и гидроксильным водородом другой молекулы.
Справочная информация – электроотрицательность атомов: С – 2,5; Н – 2,1; О – 3,5.
Распределение электронной плотности в молекулах спиртов и карбоновых кислот неравномерное:

Водородную связь в спиртах и кислотах изображают так:

В ы в о д. В гомологических рядах спиртов и карбоновых кислот отсутствуют газообразные вещества и температуры кипения веществ высокие. Это связано с наличием водородных связей между молекулами. За счет водородных связей молекулы оказываются ассоциированными (как бы сшитыми), поэтому, чтобы молекулы стали свободными и приобрели летучесть, необходимо затратить дополнительную энергию на разрыв этих связей.
4) Р а с т в о р и м о с т ь в в о д е демонстрируется экспериментально на примере растворимости в воде спиртов – этилового, пропилового, бутилового и кислот – муравьиной, уксусной, пропионовой, масляной и стеариновой. Демонстрируется также раствор муравьиного альдегида в воде.
Задание 11. Что можно сказать о растворимости спиртов, альдегидов и карбоновых кислот в воде? Чем объясняется растворимость этих веществ?
При ответе используйте схему образования водородных связей между молекулами кислоты и воды:

Необходимо отметить, что с увеличением молекулярной массы растворимость в воде спиртов и кислот уменьшается. Чем больше углеводородный радикал в молекуле спирта или кислоты, тем труднее группе ОН держать молекулу в растворе за счет образования слабых водородных связей.
Строение спиртов, альдегидов,
карбоновых кислот
Задание 12.
Аналогичную таблицу составьте дома для вторых членов гомологических рядов спиртов, альдегидов и карбоновых кислот.
Изомерии спиртов, альдегидов
и карбоновых кислот
1) И з о м е р и я с п и р т о в на примере пентанола С 5 Н 11 ОН (приведены углеродные цепи изомеров):

Задание 13. По углеродным цепям назовите разветвленные изомеры спиртов состава С 5 Н 11 ОН:

Задание 14. Являются ли данные вещества изомерами:

Задание 15. Какие виды изомерии характерны для спиртов?
2) И з о м е р и я а л ь д е г и д о в на примере н -пентаналя, или валерианового альдегида н -С 4 Н 9 СНО:

Задание 16. Какие виды изомерии характерны для альдегидов?
3) И з о м е р и я к а р б о н о в ы х к и с л о т на примере н -пентановой, или валериановой, кислоты н -С 4 Н 9 СООН:

Задание 17. Какие виды изомерии характерны для карбоновых кислот?
Задание 18. Напишите структурные формулы следующих веществ:
а) 2,4-диметил-3-этилгексаналь;
б) 2,2,4-триметил-3-изопропилпентаналь;
в) 2,3,4-триметил-3-этилпентандиол-1,2;
г) 2,3,4-триметил-3-изопропилгексантриол-1,2,4;
д) 3,4,5,5-тетраметил-3,4-диэтилгептановая кислота;
е) 2,4-диметилгексен-3-овая кислота.
Домашнее задание
Выучить тривиальные названия пяти первых альдегидов и карбоновых кислот.
Заполнить таблицу «Строение спиртов, альдегидов, карбоновых кислот» для вторых членов данных гомологических рядов (см. задание 12).
Написать все возможные изомеры для бутанола С 4 Н 10 О, бутаналя С 4 Н 8 О и бутановой кислоты С 4 Н 8 О 2 , назвать их по ИЮПАК.
Р е ш и т ь з а д а ч у. Один из многоатомных спиртов используют для приготовления антифризов – жидкостей, замерзающих при низкой температуре. Антифризы используют в зимних условиях для охлаждения автомобильных двигателей. Найдите молекулярную формулу этого спирта, если массовая доля углерода в нем составляет 38,7%, водорода – 9,7%, кислорода – 51,6%. Относительная плотность его паров по водороду равна 31. Напишите структурную формулу спирта и назовите его.
Цель: формировать умения проводить наблюдения и делать выводы, записывать уравнения соответствующих реакций в молекулярном и ионном видах.
Обеспеченность занятия
1. Сборник методических указаний для студентов по выполнению практических занятий и лабораторных работ по учебной дисциплине «Химия».
2. Раствор гидроксида натрия, карбонат натрия, карбонат кальция, оксид меди (II), уксусная кислота, лакмус синий, цинк; штатив с пробирками, водяная баня, прибор для нагревания, спички, держатель для пробирок.
Теоретический материал
Карбоновые кислоты - органические соединения, в молекулах которых содержатся одна или несколько карбоксильных групп, соединённых с углеводородным радикалом или атомом водорода.
Получение: В лаборатории карбоновые кислоты можно получить из их солей, действуя на них серной кислотой при нагревании, например:
2СН 3 – СООNa + H 2 SO 4 ® 2СН 3 – СООН + Na 2 SO 4
В промышленности получают окислением углеводородов, спиртов и альдегидов.
Химические свойства:
1. Из-за смещения электронной плотности от гидроксильной группы O–H к сильно
поляризованной карбонильной группе C=O молекулы карбоновых кислот способны к
электролитической диссоциации: R–COOH → R–COO - + H +
2.Карбоновые кислоты обладают свойствами, характерными для минеральных кислот. Они реагируют с активными металлами, основными оксидами, основаниями, солями слабых кислот. 2СH 3 COOH + Mg → (CH 3 COO) 2 Mg + H 2
2СH 3 COOH + СaO → (CH 3 COO) 2 Ca + H 2 O
H–COOH + NaOH → H–COONa + H 2 O
2СH 3 CH 2 COOH + Na 2 CO 3 → 2CH 3 CH 2 COONa + H 2 O + CO 2
СH 3 CH 2 COOH + NaHCO 3 → CH 3 CH 2 COONa + H 2 O + CO 2
Карбоновые кислоты слабее многих сильных минеральных кислот
СH 3 COONa + H 2 SO 4 (конц.) →CH 3 COOH + NaHSO 4
3. Образование функциональных производных:
a) при взаимодействии со спиртами (в присутствии концентрированной H 2 SO 4) образуются сложные эфиры.
Образование сложных эфиров при взаимодействии кислоты и спирта в присутствии минеральных кислот называется реакцией этерификации. CH 3 – –OH + HO–CH 3 D CH 3 – –OCH 3 + H 2 O
уксусная кислота метиловый метиловый эфир
спирт уксусной кислоты
Общая формула сложных эфиров R– –OR’ где R и R" – углеводородные радикалы: в сложных эфирах муравьиной кислоты – формиатах –R=H.
Обратной реакцией является гидролиз (омыление) сложного эфира:
CH 3 – –OCH 3 + HO–H DCH 3 – –OH + CH 3 OH.
Глицери́н (1,2,3-тригидроксипропан; 1,2,3-пропантриол) (гликос - сладкий) химическое соединение с формулой HOCH2CH(OH)-CH2OH или C3H5(OH)3. Простейший представитель трёхатомных спиртов. Представляет собой вязкую прозрачную жидкость.
Глицерин - бесцветная, вязкая, гигроскопичная жидкость, неограниченно растворимая в воде. Сладкий на вкус(гликос - сладкий). Хорошо растворяет многие вещества.
Глицерин этерефицируется карбоновыми и минеральными кислотами.
Эфиры глицерина и высших карбоновых кислот - жиры.
 Жиры -
это смеси сложных эфиров, образованных трехатомным спиртом глицерином и высшими жирными кислотами. Общая формула жиров, где R - радикалы высших жирных кислот:
Жиры -
это смеси сложных эфиров, образованных трехатомным спиртом глицерином и высшими жирными кислотами. Общая формула жиров, где R - радикалы высших жирных кислот:
Чаще всего в состав жиров входят предельные кислоты: пальмитиновая С15Н31СООН и стеариновая С17Н35СООН, и непредельные кислоты: олеиновая С17Н33СООН и линолевая С17Н31СООН.
Общее название соединений карбоновых кислот с глицерином - триглицериды.

б) при воздействии водоотнимающих реагентов в результате межмолекулярной
дегидратации образуются ангидриды
CH 3 – –OH + HO– –CH 3 →CH 3 – –O– –CH 3 + H 2 O
Галогенирование. При действии галогенов (в присутствии красного фосфора) образуются α-галогензамещённые кислоты:
Применение:в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров).
Вопросы для закрепления теоретического материала
1 Какие органические соединения относятся к карбоновым кислотам?
2 Почему среди карбоновых кислот нет газообразных веществ?
3 Чем обусловлены кислотные свойства карбоновых кислот?
4 Почему изменяется цвет индикаторов в растворе уксусной кислоты?
5 Какие химические свойства для глюкозы и глицерина являются общими, и чем эти вещества отличаются друг от друга? Напишите уравнения соответствующих реакций.
Задание
1. Повторить теоретический материал по теме практического занятия.
2. Ответить на вопросы для закрепления теоретического материала.
3. Исследовать свойства кислородсодержащих органических соединений.
4. Оформить отчет.
Инструкция по выполнению
1. Ознакомьтесь с правилами по технике безопасности при работе в химической лаборатории и распишитесь в журнале по ТБ.
2. Выполните опыты.
3. Результаты внесите в таблицу.
Опыт № 1 Испытание раствора уксусной кислоты лакмусом
Разбавьте полученную уксусную кислоту небольшим количеством воды и прибавьте несколько капель синего лакмуса или опустите в пробирку индикаторную бумажку.
Опыт №2 Взаимодействие уксусной кислоты с карбонатом кальция
В пробирку насыпьте немного мела (карбоната кальция) и прилейте раствор уксусной
Опыт № 3 Свойства глюкозы и сахарозы
а) В пробирку внесите 5 капель раствора глюкозы, каплю раствора соли меди (II) и при взбалтывании несколько капель раствора гидроксида натрия до образования светло - синего раствора. Такой опыт проделывали с глицерином.
б) Полученные растворы нагрейте. Что наблюдаете?
Опыт № 4 Качественная реакция на крахмал
К 5-6 каплям крахмального клейстера в пробирке прибавьте каплю спиртового раствора йода.
Образец отчёта
Лабораторная работа № 9 Химические свойства кислородсодержащих органических соединений.
Цель:формировать умения проводить наблюдения и делать выводы, записывать уравнения соответствующих реакций в молекулярном и ионном видах.
Вывод делать в соответствии с целью работы
Литература 0-2 с. 94-98
Лабораторная работа № 10
1.
2. Спирты.
А) Классификация. Определение.
Б) Изомерия и номенклатура
В) Получение спиртов
Г) Физические и химические свойства. Качественные реакции спиртов.
Д) Применение. Влияние на окружающую среду и здоровье человека.
Классификация кислородсодержащих органических соединений
1. Спирты – это кислородсодержащие органические соединения, содержащие в своем составе гидроксильную группу.
2. Альдегиды характеризуются наличием альдегидной группы:
4. Карбоновые кислоты отличает от других кислородсодержащих органических соединений карбоксильная группа.
5. Эфиры: а) простые R-O-R` б) сложные
Химические свойства этих соединений определяются наличием в их молекулах различных функциональных групп.
Класс соединений | Функциональная группа | Название функциональной группы |
гидроксильная |
||
Альдегиды | альдегидная |
|
карбонильная |
||
Карбоновые кислоты | карбоксильная |
Спирты – это кислородсодержащие производные углеводородов, в которых гидроксигруппа присоединяется к углеводородному радикалу.
Спирты классифицируются:
Ø по характеру углеродного атома, связанного с гидроксигруппой
а) первичные спирты – ОН-группа в таких соединениях связана с первичным атомом углерода
б) вторичные спирты – гидроксигруппа связана с вторичным атомом углерода
в) третичные спирты – гидроксигруппа в третичных спиртах связана с третичным углеродным атомом.
Ø по числу гидроксигрупп в молекуле спирта
а) одноатомные спирты содержат в молекуле одну ОН-группу, все представленные выше соединения являются одноатомными.
б) двухатомные – в состав таких спиртов входит две гидроксигруппы, например этиленгликоль (входит в состав незамерзающих растворов – антифризов)
https://pandia.ru/text/78/359/images/image009_3.gif" width="118" height="48 src=">
Ø по строению радикала, связанного с функциональной группой
а) насыщенные СН3-СН2-ОН (этанол)
б) ненасыщенные СН2=СН-СН2-ОН (2-пропен-1-ол)
в) ароматические Водород" href="/text/category/vodorod/" rel="bookmark">водорода в метаноле, по их старшинству с прибавлением слова-основы карбинол.


Номенклатура ИЮПАК
Согласно номенклатуре ИЮПАК:
В качестве главной цепи выбирают ту, в которой содержится наибольшее число гидроксигрупп и радикалов.
Нумерацию цепи начинают с того конца, ближе к которому находится старший заместитель – в нашем случае ОН-группа.
Название спирта строится от названия соответствующего алкана, с которым связана гидроксигруппа. Чтобы показать, что соединение относится к классу спиртов добавляется окончание –ол.
Т. к. спиртам характерна изомерия положения гидроксигруппы, то она обозначается цифрой.
Если в молекуле несколько гидроксигрупп, то их число обозначается греческими приставками (ди-, три-) Эта приставка ставится перед окончанием –ол цифрой показывается их расположение.
Например, спирты состава С4Н9ОН имеют следующее строение и названия по номенклатуре ИЮПАК.
1) соединения с нормальной цепью

2) соединения с разветвленной цепью

Таким способом называют и более сложные соединения:

Эту реакцию и ее механизм мы подробно изучили в I модуле.
Следующий промышленный способ получения спиртов – гидрирование СО.
Смесь оксида углерода (II) с водородом подвергается нагреванию. При использовании разных катализаторов продукты отличаются по составу, это иллюстрирует схема представленная ниже.

Гидролиз галогенпроизводных алканов.
Гидролиз осуществляется действием воды или водным раствором щелочей, при нагревании. Легче всего реакция проходит для первичных галогенпроизводных.

Восстановление карбонильных соединений
Альдегиды, кетоны, карбоновые кислоты и их производные (сложные эфиры) легко восстанавливаются до спиртов.
Восстановителем альдегидов и кетонов служит молекулярный водород, катализатором – никель, платина или палладий. Для восстановления эфиров используется атомарный водород, который получается при непосредственном взаимодействии натрия со спиртом.


Из уравнений видно, что из альдегидов и карбоновых кислот получаются первичные спирты, кетоны являются исходными веществами для вторичных спиртов. Так получают спирты в лабораторных условиях. Однако получить третичные спирты таким способом нельзя. Их получают способом, представленным ниже.
Взаимодействие реактивов Гриньяра с карбонильными соединениями.
Синтезы на основе реактивов Гриньяра являются надежным лабораторным способом получения спиртов.
При использовании в качестве карбонильного соединения муравьиного альдегида продуктом реакции будет первичный спирт.
Другие альдегиды приводят к образованию вторичных спиртов.
Из кетонов в таких синтезах получаются третичные спирты.
Чтобы понять, как осуществляются подобные превращения, необходимо рассмотреть электронные эффекты в реагирующих молекулах: за счет высокой электроотрицательности атома кислорода, электронная плотность смещается в сторону кислорода от углеродного атома карбонильной группы (-М-эффект). В молекуле реактива Гриньяра частично отрицательный заряд оказывается на атоме углерода, положительный – на магнии за счет положительного индуктивного эффекта (+I-эффект).
Ферментативный способ
Это сбраживание сахаристых веществ. Этанол получают брожением в присутствии дрожжей. Сущность брожения заключается том, что получаемая из крахмала глюкоза под действием ферментов распадается на спирт и СО2. результат этого процесса выражается схемой:
Физические свойства
Низкомолекулярные спирты (С1-С3) являются жидкостями с характерными запахом и вкусом и смешиваются с водой в любых соотношениях.
Температуры кипения спиртов не превышают 100°С, однако они выше чем температуры кипения эфиров или углеводородов, с такой же молекулярной массой.
Причиной этого являются межмолекулярные водородные связи, возникающие между водородными и кислородными атомами гидроксильных групп различных молекул спирта (происходит с участием неподеленных пар электронов кислорода).

Хорошая растворимость спиртов в воде объясняется образованием водородных связей между молекулами спирта и воды.
Спирты с С11 и выше – твердые вещества.
Химические свойства спиртов.
Химические свойства спиртов обусловлены присутствием гидроксигруппы. Поэтому для спиртов характерны реакции:
1) с разрывом связи –СО-Н
2) с разрывом связи С-ОН
3) реакции окисления
1. Кислотно-основные свойства спиртов.
Спирты являются амфотерными соединениями. Они способны выступать в роли как кислот, так и оснований.
Они проявляют кислотные свойства при взаимодействии со щелочными металлами и щелочами. Водород гидроксила замещается на металл с образованием алкоголятов (которые легко разлагаются водой).
2C2H5OH + 2Na = 2C2H5ONa + H2
этилат натрия
Спирты более слабые кислоты, чем вода. Их кислотные свойства в убывают в следующем порядке: СН3ОН < СН3СН2ОН < (СН3)2СНОН < (СН3)3СОН. Т. е. разветвление углеродного скелета снижает кислотные свойства.
Свойства оснований спирт проявляют по отношению к кислотам. Сильнее минеральные кислоты протонируют атом кислорода ОН-группы:

Спирты – нуклеофильные реагенты.
Реакции с карбонильными соединениями.
Спирты легко реагируют с карбоновыми кислотами, с образованием сложного эфира, такая реакция называется реакцией этерификации. Эта реакция обратима. Молекула воды образуется за счет отщепления ОН-группы от карбоновой кислоты и протона от молекулы спирта. Катализатором служит сильная минеральная кислота.
метиловый эфир уксусной кислоты
Реакции с неорганическими кислотами.
Взаимодействие спиртов с неорганическими кислотами также приводит к образованию сложных эфиров (но уже неорганических кислот).
 серноэтиловый эфир
серноэтиловый эфир
Нуклеофильное замещение гидроксигруппы .
Дегидратация спиртов.
Дегидратация спиртов протекает под действием сильных минеральных кислот (серной, ортофосфорной), при нагревании.
Отщепление может проходить внутримолекулярно . Рассмотрим механизм на примере бутанола-2: сначала происходит протонирование молекулы спирта водородом кислоты, затем отщепление воды от оксониевого иона с образованием алкил-катиона и быстрое отщепление протона с образованием алкена .

В случае отщепления Н2О применяется правило Марковникова. Это дает возможность переходить от одних спиртов к другим. Например, возможен переход от изобутилового спирта к трет-бутиловому (напишите самостоятельно)
Межмолекулярная дегидратация .
В случае межмолекулярной дегидратации продуктами реакции являются простые эфиры. Реакция протекает в тех же условиях, но отличается температурным режимом.
Окисление
Окислению подвергаются все спирт, но легче всего первичные.
Первичные спирты окисляются до альдегидов и далее до карбоновых кислот (на этой реакции основан метаболизм в организме).
Вторичные спирты в таких реакциях дают кетоны, третичные окисляются с расщеплением С-С-связи и образованием смеси кетонов и кислот.

Качественные реакции на спирты.
Как было сказано ранее, спирты могут реагировать с разрывом связей
–С –ОН и СО – Н. В качественном анализе используются и те и другие реакции.
1. Ксантогеновая проба – это наиболее чувствительная реакция на спиртовую группу. Спирт смешивают с сероуглеродом, добавляют кусочек КОН, слегка нагревают и приливают раствор CuSO4 голубого цвета. При положительной реакции возникает коричневая окраска ксантогената меди.

2 Проба Льюиса .
В реакции используется смесь концентрированной соляной кислоты и хлорида цинка. Эта реакция используется как аналитический метод установления типа спирта: является ли он первичным, вторичным или третичным.
Третичные спирты реагируют почти мгновенно с выделением тепла и образованием маслянистого слоя галогеналкана.
Вторичные реагируют в течение 5 мин (также образуется маслянистый слой).
Первичные спирты при комнатной температуре не реагируют, но вступают в реакцию при нагревании.
Применение спиртов.
Метанол применяют для производства формальдегида, уксусной кислоты, растворителя в производстве лаков и красок, служит полупродуктом для синтеза красителей, фармацевтических препаратов, душистых веществ. Сильный яд.
Этанол – сильный антисептик (в хирургии для мытья рук хирурга и инструментов) и хороший растворитель. Используется для производства дивинила (компонент каучука), хлороформа, этилового эфира (используется в медицине). Некоторое количество спирта идет на употребление в пищевой промышленности (изготовление пропитки, ликеров).
н-Пропанол применяют для производства пестицидов, лекарств, растворителя для восков, смол различной природы.
Влияние на здоровье человека. Механизм действия спиртов.
Одноатомные спирты – наркотики. Их токсичность возрастает с увеличением числа атомов углерода.
Метиловый спирт – сильный нервный и сосудистый яд, снижает насыщаемость крови кислородом. Метанол принятый внутрь взывает опьянение и тяжелое отравление сопровождаемое потерей зрения.
Метанол в пищеварительном тракте окисляется в токсичнее продукт – формальдегид и муравьиную кислоту, которые в небольших количествах взывают тяжелые отравления организма и смерть:
Этиловый спирт – наркотик, взывает паралич нервной системы.
Попадая в организм человека, спирт действует сначала возбуждающе, а затем угнетающе на ЦНС, притупляет чувствительность, ослабляет функцию головного мозга, значительно ухудшает реакцию.
Главной причиной поражения организма этанолом является образование ацетальдегида, который оказывает токсическое воздействие и взаимодействует со многими метаболитами. Ацетальдегид образуется в результате действия фермента алкогольдегидрогеназы (содержится в печени).
Пропиловый спирт действует на организм аналогично этиловому, но сильнее последнего.