Тема: Основные положения теории строения органических соединений А. М. Бутлерова.
Теория химического строения органических соединений, выдвинутая А. М. Бутлеровым во второй половине прошлого века (1861 г.), была подтверждена работами многих ученых, в том числе учениками Бутлерова и им самим. Оказалось возможным на ее основе объяснить многие явления, до той поры не имевшие толкования: , гомологию, проявление атомами углерода четырехвалентности в органических веществах. Теория выполнила и свою прогностическую функцию: на ее основе ученые предсказывали существование неизвестных еще соединений, описывали свойства и открывали их. Так, в 1862–1864 гг. А. М. Бутлеров рассмотрел пропиловых, бутиловых и амиловых спиртов, определил число возможных изомеров и вывел формулы этих веществ. Существование их позднее было экспериментально доказано, причем некоторые из изомеров синтезировал сам Бутлеров.
В течение XX в. положения теории химического строения химических соединений были развиты на основе новых воззрений, распространившихся в науке: теории строения атома, теории химической связи, представлений о механизмах химических реакций. В настоящее время эта теория имеет универсальный характер, то есть справедлива не только для органических веществ, но и для неорганических.
Первое положение. Атомы в молекулах соединяются в определенном порядке в соответствии с их валентностью. Углерод во всех органических и в большинстве неорганических соединений четырехвалентен.
Очевидно, что последнюю часть первого положения теории легко объяснить тем, что в соединениях атомы углерода находятся в возбужденном состоянии:
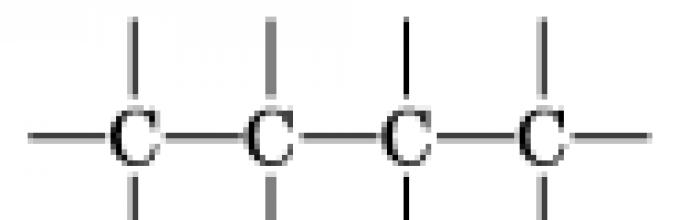
атомы четырехвалентного углерода могут соединяться друг с другом, образуя различные цепи:

Порядок соединения атомов углерода в молекулах может быть различным и зависит от вида ковалентной химической связи между атомами углерода - одинарной или кратной (двойной и тройной):

Это положение объясняет явление .
Вещества, имеющие одинаковый состав, но разное химическое или пространственное строение, а следовательно, и разные свойства, называют изомерами.
Основные виды :
Структурная изомерия, при которой вещества различаются порядком связи атомов в молекулах: углеродного скелета

![]()
![]()
![]()

![]()
![]()
Третье положение. Свойства веществ зависят от взаимного влияния атомов в молекулах.
Например, в уксусной кислоте в реакцию со щелочью вступает только один из четырех атомов водорода. На основании этого можно предположить, что только один атом водорода связан с кислородом:
С другой стороны, из структурной формулы уксусной кислоты можно сделать вывод о наличии в ней одного подвижного атома водорода, то есть о ее одноосновности.Основные направления развития теории строения химических соединений и ее значение.
Во времена А. М. Бутлерова в органической химии широко использовали
эмпирические (молекулярные) и структурные формулы. Последние отражают порядок соединения атомов в молекуле согласно их валентности, которая обозначается черточками.
Для простоты записи часто используют сокращенные структурные формулы, в которых черточками обозначают только связи между атомами углерода или углерода и кислорода.
И волокна, изделия из которых используют в технике, быту, медицине, сельском хозяйстве. Значение теории химического строения А. М. Бутлерова для органической химии можно сравнить со значением Периодического закона и Периодической системы химических элементов Д. И. Менделеева для неорганической химии. Недаром в обеих теориях так много общего в путях их становления, направлениях развития и общенаучном значении.
Теория А.М. Бутлерова
1. Атомы в молекулах соединены между собой в определенной последовательности химическими связями в соответствии с их валентностью. Порядок связи атомов называется их химическим строением. Углерод во всех органических соединениях четырехвалентен.
2. Свойства веществ определяются не только качественным и количественным составом молекул, но и их строением.
3. Атомы или группы атомов взаимно влияют друг на друга, от чего зависит реакционная способность молекулы.
4. Строение молекул может быть установлено на основании изучения их химических свойств.
Органические соединения обладают рядом характерных особенностей, которые отличают их от неорганических. Почти все они (за редким исключением) горючи; большинство органических соединений не диссоциирует на ионы, что обусловлено природой ковалентной связи в органических веществах. Ионный тип связи реализуется только в солях органических кислот, например, CH3COONa.
Гомологический ряд – это бесконечный ряд органических соединений, имеющих сходное строение и, следовательно, сходные химические свойства и отличающихся друг от друга на любое число СН2– групп (гомологическая разность).

Еще до создания теории строения были известны вещества одинакового элементного состава, но c разными свойствами. Такие вещества были названы изомерами, а само это явление – изомерией.
В основе изомерии, как показал А.М. Бутлеров, лежит различие в строении молекул, состоящих из одинакового набора атомов.
Изомерия – это явление существования соединений, имеющих одинаковый качественный и количественный состав, но различное строение и, следовательно, разные свойства.


Различают 2 вида изомерии: структурную изомерию и пространственную изомерию.
Структурная изомерия
Структурные изомеры
– соединения одинакового качественного и количественного состава, отличающиеся порядком связывания атомов, т.е химическим строением.


Пространственная изомерия
Пространственные изомеры
(стереоизомеры) при одинаковом составе и одинаковом химическом строении различаются пространственным расположением атомов в молекуле.
Пространственными изомерами являются оптические и цис-транс изомеры (геометрические).
Цис-транс-изомерия
заключается в возможности расположения заместителей по одну или по разные стороны плоскости двойной связи или неароматического цикла.В цис-изомерах заместители находятся по одну сторону от плоскости кольца или двойной связи, в транс-изомерах – по разные.

В молекуле бутена-2 СН3–СН=СН–СН3 группы СН3 могут находиться либо по одну сторону от двойной связи — в цис-изомере, либо по разные стороны — в транс-изомере.
Оптическая изомерия
Появляется тогда, когда углерод имеет четыре разных заместителя.
Если поменять местами любые два из них, получается другой пространственный изомер того же состава. Физико-химические свойства таких изомеров существенно различаются. Соединения такого типа отличаются способностью вращать плоскость пропускаемого через раствор таких соединений поляризованного света на определенную величину. При этом один изомер вращает плоскость поляризованного света в одном направлении, а его изомер – в противоположном. Вследствие таких оптических эффектов этот вид изомерии называют оптической изомерией.
Химия и фармакология
Химическое строение вещества как порядок соединения атомов в молекулах. Взаимное влияние атомов и атомных групп в молекуле. При этом строго соблюдается четырехвалентность атомов углерода и одновалентность водородных атомов. Свойства веществ зависят не только от качественного и количественного состава но и от порядка соединения атомов в молекуле явление изомерии.
§1.3. Основные положения теории химического строения органических соединений А.М.Бутлерова. Химическое строение вещества как порядок соединения атомов в молекулах. Зависимость свойств веществ от химического строения молекул. Взаимное влияние атомов и атомных групп в молекуле.
К шестидесятым годам прошлого столетия в органической химии накопился огромный фактический материал, который требовал объяснения. На фоне беспрерывного накопления экспериментальных фактов особенно остро проявлялась недостаточность теоретических представлений органической химии. Теория отставала от практики, от эксперимента. Такое отставание болезненно отражалось на ходе экспериментальных исследований в лабораториях; химики проводили свои исследования взначительной мере наугад, вслепую, зачастую не понимая природы синтезированных ими веществ и сути реакций, которые приводили к их образованию. Органическая химия, по меткому выражению Вёлера, напоминала дремучий лес, полный чудесных вещей, огромную чащу без выхода, без конца. «Органическая химия, как дремучий лес, в который легко войти, но невозможно выйти». Так, видимо, было суждено, что именно Казань дала миру компас, с которым не страшно зайти в «Дремучий лес органической химии». И этот компас, которым пользуются до сих пор Теория химического строения Бутлерова. С 60-х годов позапрошлого столетия и поныне любой в Мире учебник по органической химии начинается с постулатов теории Великого русского химика Александра Михайловича Бутлерова.
Основные положения теории химического строения
А.М. Бутлерова
1-е положение
Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям
. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой (формулой строения).
Это положение относится к строению молекул всех веществ. В молекулах предельных углеводородов атомы углерода, соединяясь друг с другом, образуют цепи. При этом строго соблюдается четырехвалентность атомов углерода и одновалентность водородных атомов.

2-е положение.
Свойства веществ зависят не только от качественного и количественного состава, но и от порядка соединения атомов в молекуле
(явление изомерии).
Изучая строение молекул углеводородов, А. М. Бутлеров пришел к выводу, что у этих веществ, начиная с бутана (С
4
Н
10
), возможен различный порядок соединения атомов при одном и том же составе молекул.Так, в бутане возможно двоякое расположение атомов углерода: в виде прямой (неразветвленной) и разветвленной цепи.

Эти вещества имеют одинаковую молекулярную формулу, но разные структурные формулы и разные свойства (температуру кипения). Следовательно, это разные вещества. Такие вещества назвали изомерами.

А явление, при котором может существовать несколько веществ, имеющих один и тот же состав и одну и ту же молекулярную массу, но различающихся строением молекул и свойствами, называют явлением изомерии. Причем с увеличением числа атомов углерода а молекулах углеводородов увеличивается число изомеров. Например, существует 75 изомеров (различных веществ), отвечающих формуле С 10 Н 22 , и 1858 изомеров с формулой С 14 Н 30 .
Для состава С
5
Н
12
могут существовать следующие изомеры (их три)-



3-е положение
.
По свойствам данного вещества можно определить строение его молекулы, а по строению - предвидеть свойства.
Доказательство данного положения.Это положение можно доказать на примере неорганической химии.
Пример. Если данное вещество изменяет окраску фиолетового лакмуса на розовый цвет, взаимодействует с металлами, стоящими до водорода, с основными оксидами, основаниями, то мы можем предположить, что это вещество относится к классу кислот, т.е. в своем составе имеет атомы водорода и кислотный остаток. И, наоборот, если данное вещество относится к классу кислот, то проявляет вышеперечисленные свойства. Например: Н
2
S
О
4
- серная кислота
4-е положение.
Атомы и группы атомов в молекулах веществ взаимно влияют друг на друга.
Доказательство данного положения
Это положение можно доказать на примере неорганической химии.Для этого надо сравнить свойства водных растворов
N
Н
3
, НС1, Н
2
О (действие индикатора). Во всех трех случаях в состав веществ входят атомы водорода, но они соединены с разными атомами, которые оказывают различное влияние на атомы водорода, поэтому свойства веществ различны.
Теория Бутлерова явилась научным фундаментом органической химии и способствовала быстрому ее развитию. Опираясь на положения теории, А.М. Бутлеров дал объяснение явлению изомерии, предсказал существование различных изомеров и впервые получил некоторые из них.
Осенью 1850 года Бутлеров сдал экзамены на ученую степень магистра химии и немедленно приступил к докторской диссертации «Об эфирных маслах», которую защитил в начале следующего года.

17 февраля 1858 года Бутлеров сделал доклад в Парижском химическом обществе, где впервые изложил свои теоретические идеи о строении вещества.Его доклад вызвал всеобщий интерес и оживленные прения:«Способность атомов соединяться друг с другом различна. Особенно интересен в этом отношении углерод, который, по мнению Августа Кекуле, является четырехвалентным, говорил в своем докладе Бутлеров Если представить валентность в виде щупальцев, с помощью которых атомы связываются между собой, нельзя не заметить, что способ связи отражается на свойствах соответствующих соединений».
Подобных мыслей никто до сих пор не высказывал. Может быть, настало время, продолжал Бутлеров, когда наши исследования должны стать основой новой теории химического строения веществ. Эта теория будет отличаться точностью математических законов и позволит предвидеть свойства органических соединений».
Через несколько лет, во время второй заграничной командировки, Бутлеров представил на обсуждение созданную им теорию Сообщение он сделал на 36-м съезде немецких естествоиспытателей и врачей в Шпейере. Съезд состоялся в сентябре 1861 года. Он выступил с докладом перед химической секцией. Тема носила более чем скромное название- «Нечто о химическом строении тел».В докладе Бутлеров высказывает основные положения своей теории строения органических соединений.
 Труды А.М. Бутлерова
Труды А.М. Бутлерова

Кабинет А.М. Бутлерова
Теория химического строения позволила объяснить многие факты, накопившиеся в органической химии в начале второй половины ХIХ в., доказала, что с помощью химических методов (синтеза, разложения и других реакций) можно установить порядок соединения атомов в молекулах (этим самым была доказана возможность познания строения вещества);
Внесла новое в атомно-молекулярное учение (порядок расположения атомов в молекулах, взаимное влияние атомов, зависимость свойств от строения молекул вещества). Теория рассматривала молекулы вещества как упорядоченную систему, наделенную динамикой взаимодействующих атомов. В связи с этим атомно-молекулярное учение получило свое дальнейшее развитие, что имело большое значение для науки химии;
Дала возможность предвидеть свойства органических соединений на основании строения, синтезировать новые вещества, придерживаясь плана;
Позволила объяснить многообразие органических соединений;
Дала мощный толчок синтезу органических соединений, развитию промышленности органического синтеза (синтез спиртов, эфиров, красителей, лекарственных веществ и др.).
Разработав теорию и подтвердив правильность ее синтезом новых соединений А.М. Бутлеров не считал теорию абсолютной и неизменной. Он утверждал, что она должна развиваться, и предвидел, что это развитие пойдет путем разрешения противоречий между теоретическими знаниями и возникающими новыми фактами.
Теория химического строения, как и предвидел А.М. Бутлеров, не осталась неизменной. Дальнейшее ее развитие шло главным образом в двух взаимосвязанных направлениях
Первое из них было предсказано самим А.М.Бутлеровым
Он считал,что наука в будущем сможет устанавливать не только порядок соединения атомов в молекуле,но и их пространственное расположение. Учение о пространственном строении молекул, называемое стереохимией (греч. «стереос» - пространственный), вошло в науку в 80-х годах прошлого столетия. Оно позволило объяснять и предсказывать новые факты, не вмещавшиеся в рамки прежних теоретических представлений.
Второе направление связано с применением в органической химии учения об электронном строении атомов, развитого в физике ХХ века. Это учение позволило понять природу химической связи атомов, выяснить сущность их взаимного влияния, объяснить причину проявления веществом тех или иных химических свойств.

Структурные формулы развернутые и краткие

Причины многообразия органических соединений
Атомы углерода образуют одинарные (простые), двойные и тройные связи:
![]()

Существуют гомологические ряды:


Изомеры:

PAGE \* MERGEFORMAT 1
А также другие работы, которые могут Вас заинтересовать |
|||
| 13229. | НЕЙСТОН І ПЕРИФІТОН | 521 KB | |
| ЛАБОРАТОРНА РОБОТА № 6 НЕЙСТОН І ПЕРИФІТОН Мета: Ознайомитись з особливостями будови та способом життя організмів нейстону і перифітону. Контрольні запитання Дати визначення поняття нейстон. Які умови необхідні для розвитку нейстону Які є два ви... | |||
| 13230. | МЕТОДИКА ПРОЕКТУВАННЯ ПРОСТИХ РЕЛЯЦІЙНИХ БАЗ ДАНИХ | 1018 KB | |
| МЕТОДИКА ПРОЕКТУВАННЯ ПРОСТИХ РЕЛЯЦІЙНИХ БАЗ ДАНИХ За матеріалами книги Glenn A. Jackson Relational Database Design With Microcomputer Applications У 1965 р. зявилися перші результати в області управління базами даних роботи Чарльза Бахмана. З тієї пори технології баз даних пройшли ве | |||
| 13231. | Учбово-відлагоджувальний стенд EV8031/AVR (V3.2) | 1.13 MB | |
| Учбово-відлагоджувальний стенд EV8031/AVR V3.2 Методичні вказівки до виконання лабораторних робіт №№ 610 ВСТУП Стенд є мікропроцесорним контроллером оснащеним памяттю програм памяттю даних і різноманітними периферійними пристроями. Він д... | |||
| 13232. | Теоретичні основи теплотехніки, Термодинаміка, теплопередача і ТСУ, Енергетичні установки | 2.88 MB | |
| Козак Ф.В. Гаєва Л.І. Негрич В.В. Войцехівська Т.Й. Демянчук Я.М. Лабораторний практикум з дисциплін Теоретичні основи теплотехніки Термодинаміка теплопередача і ТСУ Енергетичні установки Наведені загальні положення організації проведення лаборато | |||
| 13233. | Вивчення стенду, команд однокристальної ЕОМ КР1816ВЕ31 | 27.5 KB | |
| Лабораторна робота №1. Вивчення стенду команд однокристальної ЕОМ КР1816ВЕ31 Тема: Вивчення стенду команд однокристальної ЕОМ КР1816ВЕ31. Мета роботи: Вивчення функціональних можливостей учбовоналагоджувального стенду внутрішньої структури і системи команд ЕОМ КР1816ВЕ3... | |||
| 13234. | Напівпровідникові діоди | 279.5 KB | |
| Лабораторна робота №1 Тема: Напівпровідникові діоди Мета: 1. Дослідження напруги та струму діода при прямому та оберненому зміщенні рп переходу. Побудова та дослідження вольтамперної характеристики ВАХ для напівпровідникового діода. Дослідження опо | |||
| 13235. | Загальна характеристика друкарського устаткування та класифікація друкарських машин. Технологічні особливості високого та офсетного плоского способів друку | 107.5 KB | |
| ЛАБОРАТОРНА РОБОТА № 1 На тему: Загальна характеристика друкарського устаткування та класифікація друкарських машин. Технологічні особливості високого та офсетного плоского способів друку Мета: Ознайомитись із загальною характеристикою друкарського устат... | |||
| 13236. | Пристрої для виготовлення коректурних відбитків | 52 KB | |
| ЛАБОРАТОРНА РОБОТА № 2 На тему: Пристрої для виготовлення коректурних відбитків Мета роботи: вивчення технологічного процесу виготовлення коректурних відбитків у поліграфічному виконанні принципів побудови роботи вузлів і механізмів установок ФКУ і ФКУ200... | |||
| 13237. | Фотонасвітлювальні машини і автомати для запису зображень на фотоматеріалі. Фоторепродукційні апарати. Машини для оброблення фотоматеріалів | 48.5 KB | |
| ЛАБОРАТОРНА РОБОТА № 3 На тему: Фотонасвітлювальні машини і автомати для запису зображень на фотоматеріалі. Фоторепродукційні апарати. Машини для оброблення фотоматеріалів Мета роботи: вивчення технологічного процесу виготовлення текстових та ілюстраційних | |||
Все вещества, которые содержат углеродный атом, помимо карбонатов, карбидов, цианидов, тиоционатов и угольной кислоты, представляют собой органические соединения. Это значит, что они способны создаваться живыми организмами из атомов углерода посредством ферментативных или прочих реакций. На сегодняшний день многие органические вещества можно синтезировать искусственно, что позволяет развивать медицину и фармакологию, а также создавать высокопрочные полимерные и композитные материалы.
Классификация органических соединений
Органические соединения являются самым многочисленным классом веществ. Здесь присутствует порядка 20 видов веществ. Они различны по химическим свойствам, отличаются физическими качествами. Их температура плавления, масса, летучесть и растворимость, а также агрегатное состояние при нормальных условиях также различны. Среди них:
- углеводороды (алканы, алкины, алкены, алкадиены, циклоалканы, ароматические углеводороды);
- альдегиды;
- кетоны;
- спирты (двухатомные, одноатомные, многоатомные);
- простые эфиры;
- сложные эфиры;
- карбоновые кислоты;
- амины;
- аминокислоты;
- углеводы;
- жиры;
- белки;
- биополимеры и синтетические полимеры.
Данная классификация отражает особенности химического строения и наличие специфических атомных групп, определяющих разность свойств того или иного вещества. В общем виде классификация, в основе которой лежит конфигурация углеродного скелета, не учитывающая особенностей химических взаимодействий, выглядит по-другому. Соответственно ее положениям, органические соединения делятся на:
- алифатические соединения;
- ароматические вещества;
- гетероциклические вещества.
Данные классы органических соединений могут иметь изомеры в разных группах веществ. Свойства изомеров различны, хотя их атомный состав может быть одинаковым. Это вытекает из положений, заложенных А. М. Бутлеровым. Также теория строения органических соединений является руководящей основой при проведении всех исследований в органической химии. Ее ставят на один уровень с менделеевским Периодическим законом.
Само понятие о химическом строении ввел А. М. Бутлеров. В истории химии оно появилось 19 сентября 1861 года. Ранее в науке существовали различные мнения, а часть ученых вовсе отрицало наличие молекул и атомов. Потому в органической и неорганической химии не было никакого порядка. Более того, не существовало закономерностей, по которым можно было судить о свойствах конкретных веществ. При этом были и соединения, которые при одинаковом составе проявляли разные свойства.

Утверждения А. М. Бутлерова во многом направили развитие химии в нужное русло и создали для нее прочнейший фундамент. Посредством нее удалось систематизировать накопленные факты, а именно, химические или же физические свойства некоторых веществ, закономерности вступления их в реакции и прочее. Даже предсказание путей получения соединений и наличие некоторых общих свойств стало возможным благодаря данной теории. А главное, А. М. Бутлеров показал, что структуру молекулы вещества можно объяснить с точки зрения электрических взаимодействий.
Логика теории строения органических веществ
Поскольку до 1861 года в химии многие отвергали существование атома или же молекулы, то теория органических соединений стала революционным предложением для ученого мира. И поскольку сам Бутлеров А. М. исходит лишь из материалистических умозаключений, то ему удалось опровергнуть философские представления об органике.
Ему удалось показать, что молекулярное строение можно распознать опытным путем посредством химических реакций. К примеру, состав любого углевода можно выяснить посредством сжигания его определенного количества и подсчета образовавшейся воды и углекислого газа. Количество азота в молекуле амина подсчитывается также при сжигании путем измерения объема газов и выделения химического количества молекулярного азота.
Если рассматривать суждения Бутлерова о химическом строении, зависящем от структуры, в обратном направлении, то напрашивается новый вывод. А именно: зная химическое строение и состав вещества, можно эмпирически предположить его свойства. Но самое главное - Бутлеров объяснил, что в органике встречается огромное количество веществ, проявляющих разные свойства, но имеющие одинаковый состав.
Общие положения теории
Рассматривая и исследуя органические соединения, Бутлеров А. М. вывел некоторые важнейшие закономерности. Он объединил их в положения теории, объясняющей строение химических веществ органического происхождения. Положения теории таковы:
- в молекулах органических веществ атомы соединены между собой в строго определенной последовательности, которая зависит от валентности;
- химическое строение - это непосредственный порядок, согласно которому соединены атомы в органических молекулах;
- химическое строение обуславливает наличие свойств органического соединения;
- в зависимости от строения молекул с одинаковым количественным составом возможно появление различных свойств вещества;
- все атомные группы, участвующие в образовании химического соединения, имеют взаимное влияние друг на друга.

Все классы органических соединений построены согласно принципам данной теории. Заложив основы, Бутлеров А. М. смог расширить химию как область науки. Он пояснил, что благодаря тому, что в органических веществах углерод проявляет валентность равную четырем, обуславливается многообразие данные соединений. Наличие множества активных атомных групп определяет принадлежность вещества к определенному классу. И именно за счет наличия специфических атомных групп (радикалов) появляются физические и химические свойства.

Углеводороды и их производные
Данные органические соединения углерода и водорода являются самыми простыми по составу среди всех веществ группы. Они представлены подклассом алканов и циклоалканов (насыщенных углеводородов), алкенов, алкадиенов и алкатриенов, алкинов (непредельных углеводородов), а также подклассом ароматических веществ. В алканах все атомы углерода соединены только одинарной С-С связью, из-за чего в состав углеводорода уже не может быть встроен ни один атом Н.
В непредельных углеводородах водород может встраиваться по месту наличия двойной С=С связи. Также С-С связь может быть тройной (алкины). Это позволяет данным веществам вступать во множество реакций, связанных с восстановлением или присоединением радикалов. Все остальные вещества для удобства изучения их способности вступать в реакции рассматриваются как производные одного из классов углеводородов.

Спирты
Спиртами называются более сложные, чем углеводороды органические химические соединения. Они синтезируются в результате протекания ферментативных реакций в живых клетках. Самым типичным примером является синтез этанола из глюкозы в результате брожения.
В промышленности спирты получают из галогеновых производных углеводородов. В результате замещения галогенового атома на гидроксильную группу и образуются спирты. Одноатомные спирты содержат лишь одну гидроксильную групп, многоатомные - две и более. Примером двухатомного спирта является этиленгликоль. Многоатомный спирт - это глицерин. Общая формула спиртов R-OH (R - углеродная цепь).
Альдегиды и кетоны
После того как спирты вступают в реакции органических соединений, связанные с отщеплением водорода от спиртовой (гидроксильной) группы, замыкается двойная связь между кислородом и углеродом. Если данная реакция проходит по спиртовой группе, расположенной у концевого углеродного атома, то в результате ее образуется альдегид. Если углеродный атом со спиртовой расположен не на конце углеродной цепи, то результатом реакции дегидратации является получение кетона. Общая формула кетонов - R-CO-R, альдегидов R-COH (R - углеводородный радикал цепи).

Эфиры (простые и сложные)
Химическое строение органических соединений данного класса усложненное. Простые эфиры рассматриваются как продукты реакции между двумя молекулами спиртов. При отщеплении воды от них образуется соединение образца R-O-R. Механизм реакции: отщепление протона водорода от одного спирта и гидроксильной группы от другого спирта.
Сложные эфиры - продукты реакции между спиртом и органической карбоновой кислотой. Механизм реакции: отщепление воды от спиртовой и карбоновой группы обеих молекул. Водород отщепляется от кислоты (по гидроксильной группе), а сама ОН-группа отделяется от спирта. Полученное соединение изображается как R-CO-O-R, где буковой R обозначены радикалы - остальные участки углеродной цепи.
Карбоновые кислоты и амины
Карбоновыми кислотами называются особенные вещества, играющие важную роль в функционировании клетки. Химическое строение органических соединений такое: углеводородный радикал (R) с присоединенной к нему карбоксильной группой (-СООН). Карбоксильная группа может располагаться только у крайнего атома углерода, потому как валентность С в группе (-СООН) равна 4.
Амины - это более простые соединения, которые являются производными углеводородов. Здесь у любого атома углерода располагается аминный радикал (-NH2). Существуют первичные амины, у которых группа (-NH2) присоединяется к одному углероду (общая формула R-NH2). У вторичных аминов азот соединяется с двумя углеродными атомами (формула R-NH-R). У третичных аминов азот соединен с тремя углеродными атомами (R3N), где р - радикал, углеродная цепь.
Аминокислоты
Аминокислоты - комплексные соединения, которые проявляют свойства и аминов, и кислот органического происхождения. Существует несколько их видов в зависимости от расположения аминной группы по отношению к карбоксильной. Наиболее важны альфа-аминокислоты. Здесь аминная группа расположена у атома углерода, к которому присоединена карбоксильная. Это позволяет создавать пептидную связь и синтезировать белки.

Углеводы и жиры
Углеводы являются альдегидоспиртами или кетоспиртами. Это соединения с линейной или циклической структурой, а также полимеры (крахмал, целлюлоза и прочие). Их важнейшая роль в клетке - структурная и энергетическая. Жиры, а точнее липиды, выполняют те же функции, только участвуют в других биохимических процессах. С точки зрения химического строения жир является сложным эфиром органических кислот и глицерина.
К первой половине XIX века в органической химии был накоплен громадный фактический материал, дальнейшее изучение которого тормозилось отсутствием какой-либо систематизирующей основы. Начиная с 20-х годов XIX века стали появляться сменяющие друг друга теории, претендующие на обобщенное описание строения органических соединений. Одной из них была теория типов, разработанная в х годах французским ученым Ш. Жераром. Согласно этой теории, все органические соединения рассматривались как производные простейших неорганических веществ, принятых за типы.Ш. Жераром
Незадолго до появления теории строения А. М. Бутлерова немецким химиком Ф.А. Кекуле (1857) была разработана применительно к органическим соединениям теория валентности, установившая такие факты, как четырехвалентность атома углерода и его способность образовывать углеродные цепи за счет соединения с атомами углерода.А. М. БутлероваФ.А. Кекуле

Теоретические разработки добутлеровского периода внесли определенный вклад в познание строения органических соединений. Но ни одна из ранних теорий не была всеобщей. И лишь А.М. Бутлерову удалось создать такую логически завершенную теорию строения, которая и по сей день служит научной основой органической химии. Теория строения А.М. Бутлерова базируется на материалистическом подходе к реальной молекуле и исходит из возможности познания ее строения экспериментальным путем. А.М. Бутлеров при установлении строения веществ придавал основополагающее значение химическим реакциям. Теория строения А.М. Бутлерова не только объясняла уже известные факты, ее научное значение заключалось в прогнозировании существования новых органических соединений.А.М. Бутлерову А.М. Бутлерова А.М. БутлеровА.М. Бутлерова


Изомеры - это вещества, которые имеют одинаковую молекулярную формулу, но различное химическое строение, а поэтому обладают разными свойствами. Подлинное объяснение изомерия получила лишь во второй половине 19 в на основе теории химического строения А.М. Бутлерова (структурная изомерия) и стереохимического учения Я. Г. Вант-Гоффа (пространственная изомерия).Я. Г. Вант-Гоффа

ФормулаНазвание Число изомеров CH 4 метан1 C4H6C4H6 этан1 C3H8C3H8 пропан1 C 4 H 10 бутан2 C 5 H 12 пентан3 C 6 H 14 гексан5 C 7 H 16 гептан9 C 8 H 18 октан18 C 9 H 20 нонан35 C 10 H 22 декан75 C 11 H 24 ундекан159 C 12 H 26 додекан355 C 13 H 28 тридекан802 C 14 H 30 тетрадекан1 858 C 15 H 32 пентадекан4 347 C 20 H 42 эйкозан C 25 H 52 пентакозан C 30 H 62 триаконтан C 40 H 82 тетраконтан

Структурными называют изомеры, отвечающие различным структурным формулам органических соединений (с разным порядком соединения атомов). Пространственные изомеры имеют одинаковые заместители у каждого атома углерода и отличаются лишь их взаимным расположением в пространстве.

Пространственные изомеры (стереоизомеры). Стереоизомеры можно разделить на два типа: геометрические изомеры и оптические изомеры. Геометрическая изомерия характерна для соединений, содержащих двойную связь или цикл. В таких молекулах часто возможно провести условную плоскость таким образом, что заместители у различных атомов углерода могут оказаться по одну сторону (цис-) или по разные стороны (транс-) от этой плоскости. Если изменение ориентации этих заместителей относительно плоскости возможно только за счет разрыва одной из химических связей, то говорят о наличии геометрических изомеров. Геометрические изомеры отличаются своими физическими и химическими свойствами.





Открыт новый способ получения оптических изомеров органических молекул Когда Алиса оказалась в собственной, но «зазеркальной» комнате, то удивилась: комната вроде похожа, но всё же совсем другая. Точно так же различаются и зеркальные изомеры химических молекул: внешне похожи, но ведут себя по-разному. Важнейшей областью органической химии является разделение и синтез этих зеркальных вариантов. (Иллюстрация Джона Тенниела к книге Льюиса Кэрролла «Алиса в Зазеркалье»)


Американские ученые научились получать оптические изомеры соединений на основе альдегидов, осуществив наконец важную реакцию, над которой химики работали многие годы. В эксперименте они объединили два катализатора, работающие по разным принципам. В результате совместного действия этих катализаторов образуются две активных органических молекулы, которые объединяются в требуемое вещество. На примере этой реакции показана возможность синтеза целого класса биологически важных органических соединений.

Сейчас известно уже не менее 130 реакций органического синтеза, в которых получаются более или менее чистые хиральные изомеры. Если сам катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получится оптически активный продукт. Это правило было выведено еще в начале XX века и остается базовым и на сегодняшний день. Принцип выборочного действия катализатора по отношению к оптическим изомерам похож на рукопожатие: катализатору «удобно» связываться только с одним из хиральных изомеров, поэтому и катализируется предпочтительно только одна из реакций. Кстати, термин «хиральный» произошел от греческого chéir рука.